Polímeros en medicina: aplicaciones actuales y tendencias futuras
Aunque desconocidos para la gran mayoría, los polímeros son parte fundamental de la naturaleza. Su principio básico, la múltiple unión de moléculas más pequeñas denominadas monómeros, da lugar a estructuras dimensionales que están presentes en prácticamente todos los sistemas biológicos. Los polímeros naturales son indispensables para la vida tal y como la entendemos; desde las macromoléculas proteicas o nuestro propio ADN, pasando por estructuras de queratina o cartílagos, hasta la seda fabricada por algunos animales y la celulosa presente en las plantas. Han sido, además, utilizados por los humanos desde civilizaciones primigenias, con un papel básico en los primeros vestigios de la medicina, empleados, por citar algún ejemplo, como materiales de sutura [1].
Los polímeros sintéticos, por su parte, presentan una variedad cuantitativamente equiparable a la de sus homólogos naturales. Tras su primera aplicación médica durante la segunda guerra mundial, han resultado de gran interés, debido a su versatilidad. Los polímeros sintéticos pueden diseñarse a medida, permitiendo adaptar sus propiedades físico-químicas a las necesidades específicas, combinando para ello distintos monómeros y estructuras macromoleculares [2]. Las funcionalidades obtenidas ofrecen soluciones complejas como la memoria de forma [3]o la liberación controlada de compuestos respondiendo a una amplia variedad de estímulos: pH [4], estrés mecánico [5], electricidad [6]o temperatura [7].
Una ventaja asociada a los sistemas poliméricos en medicina es su estructura orgánica, basada en carbono, de similitud con los sistemas biológicos mayor que los compuestos inorgánicos [8]. Esta particularidad es de gran interés al buscar una interacción específica del polímero con el cuerpo. Sin embargo, puede también conllevar una serie de problemas asociados a la presencia de restos de monómeros [9], procesos degradativos indeseados o aditivos con respuesta bioquímica [10].
Por otro lado, la posibilidad de introducir grupos reactivos en las estructuras poliméricas permite su anclaje a otras superficies [11], ofreciendo la posibilidad de modificar superficialmente otros materiales con propiedades intrínsecas interesantes para una aplicación determinada. Así, pueden regularse propiedades como la biocompatibilidad [12]o favorecer la proliferación de determinado tipo de células [13].
Los distintos polímeros sintéticos empleados son variados, siendo las familias de las poliolefinas [14], poliésteres [15], poliéteres [16], polímeros fluorados [17], vinílicos [18], acrílicos [19], poliamidas [20], poliuretanos [21] y siliconas [22] los más empleados. El portfolio disponible aumenta día a día y la irrupción de nuevas tecnologías como la impresión 3D, junto con la digitalización que engloba a todos los sectores, promete un horizonte esperanzador para la ya de por sí potente industria asociada. No en vano, de acuerdo a la consultora Grand View Research, en 2016 el mercado global asociado a los polímeros para el sector médico se estimaba en más de 12.000 millones de dólares, con un crecimiento interanual superior al 8% y se espera que supere la barrera de los 17.000 millones de dólares para el año 2020.
Aplicaciones que no implican contacto con el cuerpo
La principal aplicación se centra en embalaje, contenedores y dispositivos médicos. Con requisitos mucho menos restrictivos que en los casos posteriores, se deben tener en cuenta, no obstante, parámetros relacionados con el contacto entre el polímero y los compuestos activos que portan, suministran o dosifican [23], tal y como su posible interacción. El objetivo es asegurar que la funcionalidad de ninguno de los dos se vea comprometida. De este modo, deberán ser consideradas las migraciones del compuesto activo a la matriz polimérica, cambios de pH, permeación de gases, propiedades ópticas o migración de aditivos [24], entre otros.
El policloruro de vinilo (PVC) ha sido uno de los materiales más empleados para estos usos, sin embargo, la adición de plastificantes para adecuar sus propiedades mecánicas [25], generalmente ftalatos con alta lipofilia, conocidos por su efecto carcinogénico y actividad endocrina, supone un riesgo de migración. Por ello, las poliolefinas, inertes y fácilmente formulables, son el material más empleado para este tipo de aplicaciones en la actualidad [26]. Polietileno (PE) y polipropileno (PP) se utilizan como único material o en formato multicapa, junto con materiales que mejoran las propiedades de barrera y protegen de radiación lumínica al principio activo.
Otras aplicaciones extracorporales habituales son las membranas para hemodiálisis [27], fabricadas en una combinación de polímeros hidrófobos e hidrófilos, como poliaril sulfonas, polisufonas, poliétersulfonas o polivinil pirrolidona. También son comunes aquellas aplicaciones dedicadas al transporte de diferentes fluidos, donde elastómeros de poliuretano (TPU) y siliconas son los materiales con mayor presencia.
Aplicaciones in vivo temporales
Como se ha expuesto anteriormente, la versatilidad de los polímeros permite cubrir una serie de necesidades muy específicas y concretas. Éste es el caso de los catéteres, que requieren una flexibilidad y propiedades mecánicas críticas para su correcto desempeño. Los catéteres vasculares, inicialmente fabricados en PVC, han sido a día de hoy sustituidos por TPU y siliconas [21],21 debido a los problemas de migración ya mencionados [25]25. Éstos, a su vez, incluyen aditivos antimicrobianos o son funcionalizados superficialmente con cadenas poliméricas altamente hidrófilas, como el polietilen glicol (PEG), para evitar la adsorción de proteínas en superficie. Otros materiales empleados en catéteres son el polietileno de alta densidad (HDPE) o politetrafluoroetileno (PTFE), debido a su bajo coeficiente de rozamiento, que facilita su inserción como catéter guía, así como poliésteres o poliamidas (PA) habitualmente empleados en balones para dosificación.
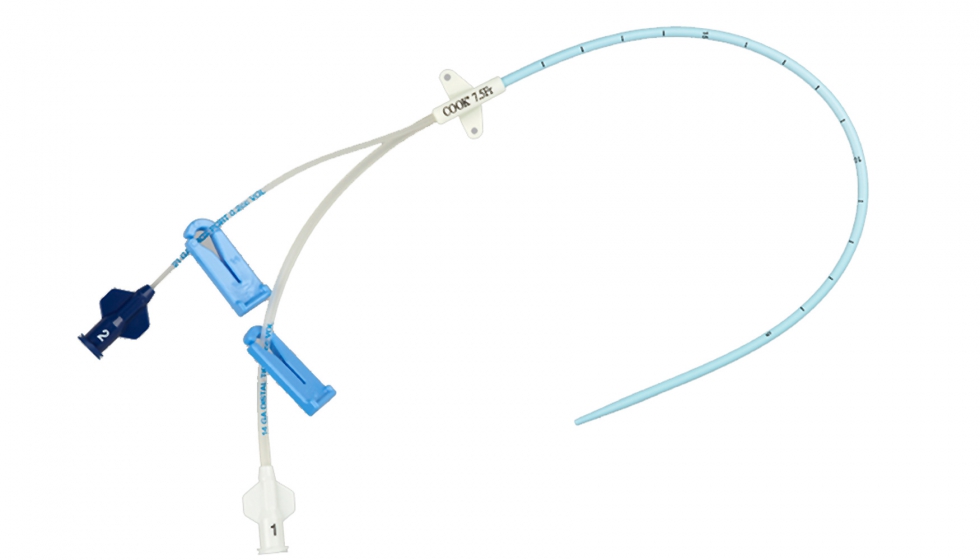
En lo que a catéteres urinarios se refiere, las siliconas son el material prevalente [28]. Estas son aditivadas con diferentes compuestos antimicrobianos con el objetivo de asegurar un uso prolongado de los catéteres libres de infecciones, si bien es un problema no resuelto, observándose signos de infección en casi el 100% de los pacientes tras más de 30 días de uso continuado [29].
Los apósitos también son un amplio campo de aplicación. Comparados con los tradicionales, aquellos de base polimérica permiten una óptima protección mecánica y buenas propiedades barrera, con mínima adherencia a la herida mejorando el proceso de cura y retirada para el paciente [30]. Han despertado últimamente especial interés los apósitos híbridos que combinan polímeros sintéticos y naturales [31]; por ejemplo, films semi impermeables de nylon (PA) y poliuretanos con recubrimientos acrílicos o de quitosano, con excelentes propiedades frente a heridas que requieren una correcta humectación [32]. De igual manera, las gasas activas capaces de absorber gran cantidad de líquido son de gran interés para tratar quemaduras y otras heridas supurantes [30].30 Los hidrocoloides poliméricos y derivados celulósicos, por su parte, evitan la proliferación de microorganismos y aceleran el proceso de sanación, gracias a la liberación controlada de fármacos [33] cicatrizantes o antisépticos.
En otro orden, y en contacto con la piel de forma intermitente, nos encontraríamos con órtesis y prótesis externas para, por ejemplo, miembros amputados. La irrupción de los materiales poliméricos en el sector supuso una revolución en cuanto a prestaciones para el paciente. El uso de liners de poliuretano o silicona [34] y de resina reforzada con

fibra de carbono para encajes o pies almacenadores de energía ha permitido reducir el peso de las prótesis y ha aumentado el confort general de los pacientes, barriendo gran parte de sus limitaciones. Adicionalmente, la incursión de la impresión 3D ha permitido personalizar las prótesis convirtiéndolas en un elemento de moda más, eliminando el estigma del amputado en gran medida [35].
Aplicaciones quirúrgicas generales
Desde que se empleara el polimetil metacrilato para reparar daños en la córnea de soldados alemanes durante la II Guerra Mundial, se comprobó el potencial de los polímeros en usos en implantes y todo tipo de cirugías invasivas. De todos ellos, no obstante, el campo preferente ha sido el de las suturas. Hoy en día, además de fibras poliméricas sintéticas de poliéster, poliamida o polietileno y naturales no reabsorbibles como algodón o seda [36], son habituales las suturas bioabsorbibles basadas en polímeros biodegradables como ácido poliláctico (PLA), ácido poliglicólico (PGA), policaprolactona (PCL) y copolímeros de los mismos con diferentes ácidos naturales [37]. En este sentido, la eclosión de los polímeros ha permitido encontrar soluciones adhesivas [38] capaces de sustituir satisfactoriamente a las suturas en muchos casos. Los adhesivos más clásicos se basan en una evolución de los convencionales compuestos por poliuretanos, derivados de isocianatos y poliésteres biodegradables y reabsorbibles como la PCL [39]. Entre los más empleados actualmente se encuentran polímeros basados en fibrina y trombina, si bien las alternativas incipientes basadas en heparina, gelatina, colágeno o diversos polisacáridos de origen natural o sintético [40]son cada vez mayores.
Por otro lado, son de uso habitual también las mallas quirúrgicas [41], basadas en polímeros altamente inertes y de baja fricción como el PP, PTFE que poco a poco están siendo sustituidas por las mallas de polifluoruro de vinilideno (PVDF) debido a una respuesta de rechazo inferior [42].
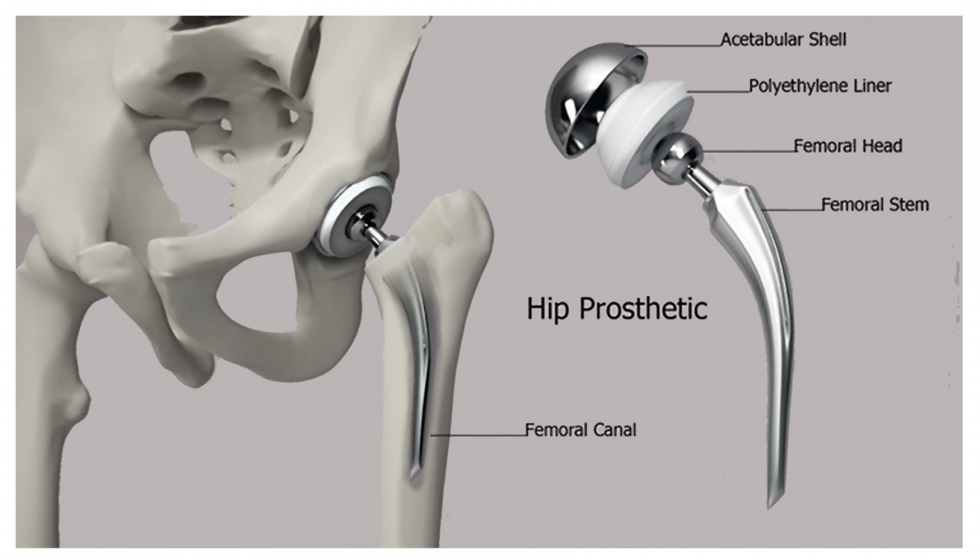
Finalmente, cabe destacar toda una serie de aplicaciones quirúrgicas implantadas desde hace años, aunque no por ello menos importantes. Estas aplicaciones médicas no son otras que el uso de polietilenos de ultra alta densidad (UHMWDPE) en las prótesis de cadera [43], o los cementos óseos basados en polímeros acrílicos [44] empleados en su implantación, así como los stents fabricados con poliésteres biodegradables [45] o válvulas cardíacas basadas en TPU [46]. Tampoco se pueden pasar por alto las contribuciones al sector oftálmico [47] y dental [48] donde los polímeros acrílicos han revolucionado la manera de entender ambas industrias.
Conclusiones
Resumiendo, podríamos argumentar que la irrupción de los polímeros en la medicina está aún en una etapa incipiente, aunque prometedora. La propia versatilidad intrínseca de estos materiales los convierte en los candidatos perfectos para abordar la gran cantidad de retos presente en un sector tan exigente como el médico. La revolución digital y las nuevas tecnologías productivas como la impresión 3D, en la que los materiales poliméricos se presentan como uno de los ejes centrales, servirán como palanca clave. Todo ello permite afirmar que la penetración de los polímeros en el sector médico tendrá lugar en diversas formas y atacando diferentes frentes, en los que el material podrá ser portador de fármacos, material estructural o el propio principio activo. No obstante, su implementación aún presenta ciertas dudas desde el punto de vista de regulación y toxicidad, debido a que el escaso bagaje no permite tener una base de datos equiparable a otros materiales. Es, por tanto, trabajo de la comunidad científica e industrial sentar las bases y herramientas necesarias para explotar, de forma segura y eficiente, todas las posibilidades que estos materiales camaleónicos pueden ofrecer.
Referencias
[1] T.M. Muffly, A.P. Tizzano, M.D. Walters, The history and evolution of sutures in pelvic surgery, J. R. Soc. Med. 104 (2011) 107-112.
[2] A. Lendlein, Polymers in biomedicine, Macromol. Biosci. 10 (2010) 993-997.
[3] A. Lendlein, M. Behl, B. Hiebl, C. Wischke, Shape-memory polymers as a technology platform for biomedical applications, Expert Rev. Med. Devices 7 (2010) 357-379.
[4] S. Dai, P. Ravi, K.C. Tam, pH-Responsive polymers: synthesis, properties and applications, Soft Matter 4 (2008) 435-449.
[5] C. Weder, Mechanochemistry: Polymers react to stress, Nature 459 (2009) 45-46.
[6] Q. Yan, J. Yuan, Z. Cai, Y. Xin, Y. Kang, Y. Yin, Voltage-responsive vesicles based on orthogonal assembly of two homopolymers, J. Am. Chem. Soc. 132 (2010) 9268-9270.
[7] D.F. Stamatialis, B.J. Papenburg, M. Giron.s, S. Saiful, S.N.M. Bettahalli, S. Schmitmeier, M. Wessling, Medical applications of membranes: Drug delivery, artificial organs and tissue engineering, J. Memb. Sci. 308 (2008) 1-34.
[8] Catauro, M., et al. Influence of the polymer amount on bioactivity and biocompatibility of SiO2/PEG hybrid materials synthesized by solgel technique. Materials Science and Engineering: C 48 (2015): 548-555.
[9] Langer, Robert, and David A. Tirrell. Designing materials for biology and medicine. Nature 428.6982 (2004): 487.
[10] M.D. Smith, M.H. Grant, C.R. Blass, J.M. Courtney, J.C. Barbenel, Poly(vinyl chloride) formulations: acute toxicity to cultured human cell lines, J. Biomater. Sci. Polym. Ed. 7 (1995) 453-459.
[11] Kulkarni, Mukta, et al. Biomaterial surface modification of titanium and titanium alloys for medical applications. Nanomedicine 111 (2014): 111.
[12] LaPorte, R. (1997). Hydrophilic Polymer Coatings for Medical Devices. New York: Routledge.
[13] Shi, Changcan, et al. Hydrophilic PCU scaffolds prepared by grafting PEGMA and immobilizing gelatin to enhance cell adhesion and proliferation. Materials Science and Engineering: C 50 (2015): 201-209.
[14] Kim, Yong K. The use of polyolefins in industrial and medical applications. Polyolefin Fibres (Second Edition). 2017. 135-155.
[15] S. Kehoe, X.F. Zhang, D. Boyd, FDA approved guidance conduits and wraps for peripheral nerve injury: a review of materials and efficacy, Injury 43 (2012) 553-572.
[16] S.M. Kurtz, J.N. Devine, PEEK biomaterials in trauma, orthopedic, and spinal implants, Biomaterials 28 (2007) 4845-4869.
[17] A.S. Breitbart, V.J. Ablaza, Implant materials, in: C.H. Thorne (Ed.) Grabb and Smith's Plastic Surgery, Lippincott Williams & Wilkins, Philadelphia, Pa., 2007, pp. 58-65.
[18] J. Sampson, D. de Korte, DEHP-plasticised PVC: relevance to blood services, Transfus. Med. 21 (2011) 73-83.
[19] M. Tanaka, A. Mochizuki, Clarification of the blood compatibility mechanism by controlling the water structure at the blood-poly(meth)acrylate interface, J. Biomater. Sci. Polym. Ed. 21 (2010) 1849-1863.
[20] L. Pruitt, J. Furmanski, Polymeric biomaterials for load-bearing medical devices, JOM 61 (2009) 14-20.
[21] C. ONeil, So many polymers, so little time, MD+DI 32 No. 9 (2010) http://www.mddionline.com/article/so-many-polymers-so-little-time.
[22] P.J. Mackenzie, R.M. Schertzer, C.M. Isbister, Comparison of silicone and polypropylene Ahmed glaucoma valves: two-year follow-up, Can. J. Ophthalmol. 42 (2007) 227-232.
[23] D.R. Jenke, Extractables and leachables considerations for prefilled syringes, Expert Opin. Drug Deliv. 11 (2014) 1591-1600.
[24] D. Jenke, Evaluation of the chemical compatibility of plastic contact materials and pharmaceutical products; safety considerations related to extractables and leachables, J. Pharm. Sci. 96 (2007) 2566-2581.
[25] J. Sampson, D. de Korte, DEHP-plasticised PVC: relevance to blood services, Transfus. Med. 21 (2011) 73-83.
[26] S. Makwana, B. Basu, Y. Makasana, A. Dharamsi, Prefilled syringes: An innovation in parenteral packaging, Int. J. Pharm. Investig. 1 (2011) 200-206.
[27] N.A. Hoenich, Membranes for dialysis: can we do without them?, Int. J. Artif. Organs 30 (2007) 964-970.
[28] E.L. Lawrence, I.G. Turner, Materials for urinary catheters: a review of their history and development in the UK, Med. Eng. Phys. 27 (2005) 443-453.
[29] K.H. Dellimore, A.R. Helyer, S.E. Franklin, A scoping review of important urinary catheter induced complications, J. Mater. Sci. Mater. Med. 24 (2013) 1825-1835.
[30] G.D. Mogosanu, A.M. Grumezescu, Natural and synthetic polymers for wounds and burns dressing, Int. J. Pharm. 463 (2014) 127-136.
[31] K.C. Broussard, J.G. Powers, Wound dressings: selecting the most appropriate type, Am. J. Clin. Dermatol. 14 (2013) 449-459.
[32] N. Mayet, Y.E. Choonara, P. Kumar, L.K. Tomar, C. Tyagi, L.C. Du Toit, V. Pillay, A comprehensive review of advanced biopolymeric wound healing systems, J. Pharm. Sci. 103 (2014) 2211-2230.
[33] J.S. Boateng, K.H. Matthews, H.N.E. Stevens, G.M. Eccleston, Wound healing dressings and drug delivery systems: A review, J. Pharm. Sci. 97 (2008) 2892-2923.
[34] Baars, E. C. T., and J. H. B. Geertzen. Literature review of the possible advantages of silicon liner socket use in trans-tibial prostheses. Prosthetics and orthotics international 29.1 (2005): 27-37.
[35] http://unyq.com/prosthetic-covers/
[36] F. Javed, M. Al-Askar, K. Almas, G.E. Romanos, K. Al-Hezaimi, Tissue reactions to various suture materials used in oral surgical interventions, ISRN Dent. 2012 (2012) 762095.
[37] I. Capperauld, Suture materials: A review, Clin. Mater. 4 (1989) 3-12.
[38] L. Sanders, J. Nagatomi, Clinical applications of surgical adhesives and sealants, Crit. Rev.
Biomed. Eng. 42 (2014) 271-292.
[39] P. Ferreira, A.F.M. Silva, M.I. Pinto, M.H. Gil, Development of a biodegradable bioadhesive containing urethane groups, J. Mater. Sci. Mater. Med. 19 (2008) 111-120.
[40] L.P. Bre, Y. Zheng, A.P. Pego, W.X. Wang, Taking tissue adhesives to the future: from traditional synthetic to new biomimetic approaches, Biomater. Sci. 1 (2013) 239-253.
[41] U. Klinge, J.K. Park, B. Klosterhalfen, 'The ideal mesh?', Pathobiology 80 (2013) 169-175.
[42] K. Junge, M. Binnebosel, K.T. von Trotha, R. Rosch, U. Klinge, U.P. Neumann, P.L. Jansen, Mesh biocompatibility: effects of cellular inflammation and tissue remodelling, Langenbecks Arch. Surg. 397 (2012) 255-270.
[43] M.J. Kasser, Regulation of UHMWPE biomaterials in total hip arthroplasty, J. Biomed. Mater. Res. B Appl. Biomater. 101B (2013) 400-406.
[44] J. Wang, C. Zhu, T. Cheng, X. Peng, W. Zhang, H. Qin, X. Zhang, A systematic review and metaanalysis of antibiotic-impregnated bone cement use in primary total hip or knee arthroplasty, PLoS One 8 (2013) e82745.
[45] T. Palmerini, G. Biondi-Zoccai, D. Della Riva, A. Mariani, M. Sabate, P.C. Smits, C. Kaiser, F. D'Ascenzo, G. Frati, M. Mancone, P. Genereux, G.W. Stone, Clinical outcomes with bioabsorbable polymer-versus durable polymer-based drug-eluting and bare-metal stents evidence from a comprehensive network meta-analysis, J. Am. Coll. Cardiol. 63 (2014) 299-307.
[46] A. Abruzzo, C. Fiorica, V.D. Palumbo, R. Altomare, G. Damiano, M.C. Gioviale, G. Tomasello, M. Licciardi, F.S. Palumbo, G. Giammona, A.I. Lo Monte, Using polymeric scaffolds for vascular tissue engineering, Int. J. Polym. Sci. (2014).
[47] S. Kirchhof, A.M. Goepferich, F.P. Brandl, Hydrogels in ophthalmic applications, Eur. J. Pharm. Biopharm. (2015) doi:10.1016/j.ejpb.2015.05.016
[48] J.G. Leprince, W.M. Palin, M.A. Hadis, J. Devaux, G. Leloup, Progress in dimethacrylate-based dental composite technology and curing efficiency, Dent. Mater. 29 (2013) 139-156.