Eliminación y determinación de fosfato

Fosfato en el agua: origen y eliminación
Los compuestos del fósforo son nutrientes de las plantas y conducen al crecimiento de algas en las aguas superficiales. Dependiendo de la concentración de fosfato existente en el agua, puede producirse la eutrofización. Tan sólo 1 gramo de fosfato-fósforo (PO4-P) provoca el crecimiento de hasta 100 g de algas. Cuando estas algas mueren, los procesos de descomposición dan como resultado una demanda de oxígeno de alrededor de 150 gramos. Las concentraciones críticas para una eutrofización incipiente se encuentran entre 0,1-0,2 mg/l PO4-P en el agua corriente y entre 0,005-0,01 mg/l PO4-P en aguas tranquilas. En vista del peligro potencial para las aguas superficiales, la directiva EU 91/271/CEE especifica unos valores límite para el vertido de compuestos de fosfato a las aguas receptoras. En función del tamaño de la EDAR, estos valores son 2 mg/l P total (10.000 100.000 h-e) o 1 mg/l P total (> 100.000 h-e).
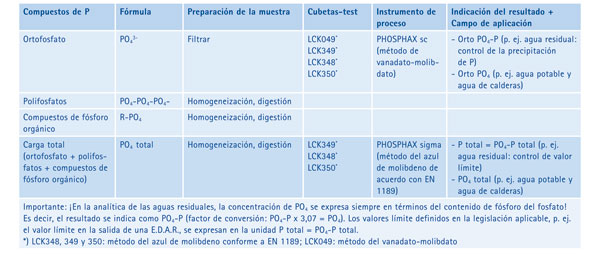
¿De dónde viene el fosfato?
Los compuestos de fosfato que se encuentran en las aguas residuales o se vierten directamente a las aguas superficiales provienen de:
- Fertilizantes eliminados del suelo por el agua o el viento
- Excreciones humanas y animales
- Detergentes y productos de limpieza
La carga de fosfato total se compone de ortofosfato + polifosfato + compuestos de fósforo orgánico, siendo normalmente la proporción de ortofosfato la más elevada.
Los fosfatos existen en forma disuelta, coloidal o sólida. Antes de realizar un análisis, por tanto, es importante considerar qué tipo de fosfatos deberán determinarse. Si solamente se va a determinar ortofosfato (por ejemplo para el control de la precipitación de fósforo), sólo hay que filtrar la muestra antes de analizarla. Sin embargo, si se va a determinar la concentración de fósforo total (por ejemplo, para el control de los valores límite), primero hay que homogeneizar la muestra y después hidrolizarla (someterla a digestión).

Eliminación de fosfato
Hoy en día, puede suponerse que la concentración media en la entrada de una depuradora municipal es de 9 miligramos de fósforo en total. Esta concentración debe reducirse, durante los procesos de depuración del agua residual, hasta el valor límite en la salida especificado legalmente. Existen dos modos de llevar esto a cabo: la eliminación biológica de fósforo o la precipitación química de fosfato. Las desventajas asociadas a los métodos de precipitación son el aumento de la salinidad del agua residual (y por tanto también del agua receptora) y el constante aumento del precio de los precipitantes. Además, las sales de fosfato precipitadas llevan al aumento del volumen de fango. Por este motivo, en la práctica se utiliza una combinación de eliminación biológica y química de fósforo para minimizar el consumo de precipitante.
Eliminación biológica de fósforo
Almacenamiento de más fosfato del normalmente necesario en el fango activo floculado. Esto se produce cuando el fango está en un entorno unas veces aeróbico y otras veces anaeróbico (entrada de oxígeno activada/ desactivada). La eliminación biológica eficaz de fósforo depende de la presencia de suficientes materias orgánicas fácilmente biodegradables (DBO5). Una relación P/DBO5 de < 0,03 y una relación N/DBO5 de < 0,25 en la entrada del tanque de aireación favorecen el aumento de la degradación biológica de fósforo.
Precipitación química de fosfato
Los compuestos de ortofosfato son precipitados como fosfatos de metales difícilmente solubles con la ayuda de productos químicos (sales de hierro o de aluminio, lechada de cal). Las sales se sedimentan y permanecen en el lodo de las aguas residuales. El precipitante se puede agregar durante el tratamiento primario (pre-precipitación) o en el tanque de aireación (precipitación simultánea), o en un tanque de reacción adicional aguas abajo del tanque de aireación (postprecipitación). El método más utilizado es la precipitación simultánea, ya que se trata de la variante más económica.
Análisis de fosfato
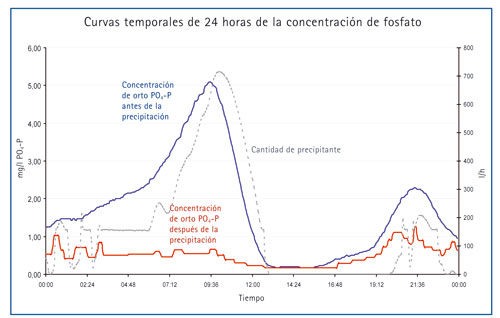
Para el control y la comprobación de la eliminación de P y controlar los valores límite son necesarios unos análisis periódicos en varios puntos de medida del proceso de tratamiento del agua residual. Además, la adición selectiva de precipitantes en función de la carga de fósforo puede conllevar ahorros de costes. La determinación de PO4-P puede realizarse en el laboratorio con una cubeta-test o en continuo mediante un instrumento de medida de proceso. Por regla general, se registran unas curvas temporales, (p. ej. durante un periodo de 24 horas) en un único punto de medida, con el fin de obtener una vista exacta de la magnitud de la carga de PO4. La adición necesaria de precipitante se puede entonces regular partiendo de la curva (véase la figura 1). Más efectiva es la medida en continuo de la concentración de PO4-P con una conexión directa a los sistemas dispensadores de precipitante.
Causas de concentraciones elevadas de PO4-P en el efluente, y remedios
Causas y soluciones posibles:
- Se está añadiendo muy poco precipitante, o éste se está agregando en un punto poco favorable: controlar la adición de precipitante y aumentar la cantidad a adicionar o agregar el precipitante en otro punto
- El fósforo se está redisolviendo en el decantador secundario: la concentración de orto PO4-P en la salida del decantador secundario es mayor que en la etapa de nitrificación y se ha de aumentar el contenido de oxígeno en la etapa de nitrificación o aumentar la relación de lodo de recirculación.

Causas y soluciones posibles:
- Proporción de sólidos demasiado alta, provocada por la pérdida de lodo: flóculos o estructura del fango activado demasiado ligeros, pequeños o filamentosos en combinación con sobrecargas hidráulicas (lluvia, deshielo). Se ha de controlar la capacidad ácida en el tanque de aireación o adoptar medidas para combatir los lodos no sedimentables
- Existen polifosfonatos difícilmente degradables, posiblemente procedentes de agentes de limpieza industriales: esta situación sólo se puede mejorar mediante una eliminación en el punto donde tiene lugar, pues los precipitantes no reaccionan con tales compuestos.







































