Inmunoterapias: la puerta de la esperanza

¿El cambio? El enfoque, que pasa de centrase en el estudio del tumor a contemplar su entorno más allá del tejido anómalo, y uno de los elementos de ese entorno es el sistema inmune; su estimulación es el objeto de diversas terapias cuyas particularidades ponen sobre el tapete algunas cuestiones técnicas, económicas, éticas equidad a la hora de acceder a ellas y legislativas de no poca entidad. A corto plazo, probablemente no será un gran número de pacientes el que se beneficie de estas terapias, muy personalizadas y, por el momento, caras.
En cualquier caso, la envergadura del objeto de estudio; su carácter holístico y multidisciplinar, no en vano el sistema inmune se encuentra en conexión con todo nuestro organismo; la complejidad para determinar sus mecanismos de acción e identificar dianas terapéuticas, para una intervención dirigida, y para el establecimiento de las dosis y de las combinaciones terapéuticas en cada caso, hacen que el éxito de la inmunoterapia dependa de cómo se organice la comunidad científica a escala mundial para poner en común sus investigaciones; en definitiva, de los medios con los que cuente. Porque esta batalla, y muchas otras, se ganará si como sociedad priorizamos el conocimiento en todos los ámbitos: the knowledge, first!
Se llama Emily Whitehead. Seguramente el nombre no les suene, pero su impresionante curación de una leucemia linfoblástica aguda a los 6 años después de ser tratada con una terapia génica y celular, entonces experimental, CAR-T (inmunoterapia con células T un tipo de linfocitos con receptor de antígeno quimérico CAR), abrió las puertas a un nuevo frente en la lucha contra algunas de las enfermedades más mortales de nuestra sociedad. Desde entonces, la comunidad científica ha puesto el foco sobre una línea de investigación que había quedado aparcada durante demasiado tiempo: nuestro, casi perfecto, sistema inmune.

Los progresos se han sucedido desde entonces. Con el llamado Paciente de Berlín, el primer caso de curación del sida (al cierre de esta edición se acaba de confirmar el segundo caso, en Londres) después de un trasplante de células madre en 2007 y otro en 2008 con motivo de un diagnóstico adicional de leucemia de la que también se curó, se constataba la influencia del sistema inmune del donante, de sus linfocitos T, en el control del virus (el donante tenía una mutación genética que confiere resistencia a la infección de VIH). En 2018, una inmunoterapia logra curar un cáncer de mama metastásico, extrayendo linfocitos del tumor, identificando los más activos (pero insuficientes en número), multiplicándolos en el laboratorio y reinfundiéndolos a la paciente, que se curó completamente con sus propias células inmunes. Esto nos da una idea del grado de personalización que requiere este tipo de tratamientos que, por otra parte, no funcionan en todos los pacientes ni en todos los tipos de tumor; y ahí es donde se centran ahora las investigaciones.
Aunque para asomarnos a los orígenes del fundamento de las inmunoterapias tenemos que retroceder más de un siglo, cuando el cirujano y oncólogo neoyorquino William Coley observó que el índice de supervivencia tras la cirugía de un tumor, era mayor cuando se producía una infección, y en 1891experimentó por primera vez inyectando bacterias de erisipela directamente en un tumor, que, en efecto, se redujo.
Siempre ha habido científicos que han creído en la capacidad del sistema inmune para erradicar el cáncer, apunta Elena Garralda, directora ejecutiva de la UITM (Unidad de Investigación de Terapia Molecular) e investigadora principal del Grupo de Desarrollo Clínico Precoz de Fármacos del Hospital Vall dHebron Instituto de Oncología. En el mismo sentido se expresa Manel Juan, jefe de la Sección de Inmunoterapia del Servicio de Inmunología del Hospital Clínic de Barcelona y responsable de la Plataforma de Inmunoterapia Hospital Sant Joan de Deu-Hospital Clínic: Evidencias existen desde hace mucho tiempo, más allá de situaciones en las que encontramos tumores que de manera espontanea desparecen, y que alguna vez se ha querido relacionar con creencias, pero el principal factor al que se atribuye este tipo de curaciones es al sistema inmunológico.
En los últimos tiempos las noticias sobre los avances en el ámbito de la inmunoterapia se suceden a ritmo vertiginoso y aunque los principales logros se han obtenido en oncología, ya que hasta ahora estos tratamientos se han venido utilizando como último recurso en pacientes sin otras opciones terapéuticas, de estos continuos hallazgos pueden beneficiarse todas las enfermedades mediadas por el sistema inmunitario como las alergias o las enfermedades autoinmunes, como la artritis reumatoide, explica Juan. En la actualidad los cánceres más susceptibles de ser tratados con inmunoterapia son los de piel, pulmón y de la sangre (leucemias y linfomas).
Los ensayos clínicos se cuentan por cientos en todo el mundo, y algunas de estas terapias ya se están utilizando, también en España. El Gobierno ha anunciado recientemente que financiará las dos primeras terapias CAR-T comerciales: el Kymriah, de Novartis, con quien ya ha llegado a un acuerdo económico basado en el pago por resultados, y el Yescarta, de Kite Pharma, ambos aprobados por la EMA el verano pasado, para tratar la leucemia linfoblástica aguda (LLA) en pacientes pediátricos y jóvenes hasta los 25 años, y para el linfoma de linfocitos B en adultos, respectivamente. Paralelamente, el Estado financiará una terapia CAR-T pública para la LLA, que fabricará el Hospital Clínic de Barcelona y que será como las comerciales pero, presumiblemente, más barata.
Sin duda, 2018 ha sido el año de las inmunoterapias, y así se ha reconocido con la concesión del Novel de Medicina a los descubridores de los frenos moleculares PD1 y CTLA-4.
Los tratamientos basados en inmunoterapia constituyen una herramienta adicional a los tratamientos tradicionales, como la cirugía, la radioterapia y la quimioterapia, pero con muchos menos efectos secundarios, y abren la puerta a hacer realidad la aspiración de convertir los cánceres y otras dolencias hoy mortales, cuando menos, en enfermedades crónicas.
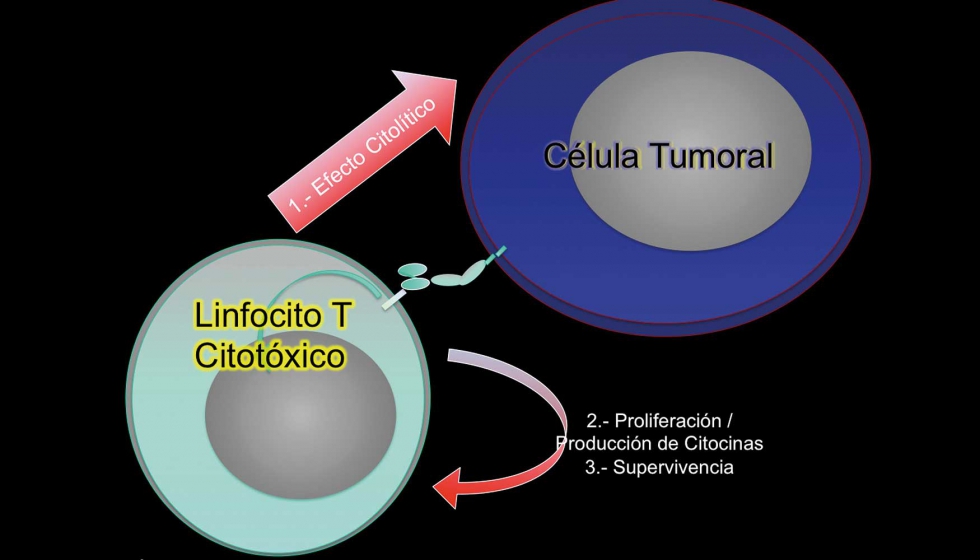
Arranca la gran batalla
El cometido de nuestro sistema inmune es protegernos frente a patógenos, como los virus, también eliminando o suprimiendo las infecciones virales causantes de tumores o la inflamación, que puede resultar un entorno favorecedor para el desarrollo de tumores. Las células inmunitarias, los linfocitos, circulan por todo nuestro organismo buscando, mediante unos receptores, elementos extraños, como bacterias o virus, y una vez detectados se activan las denominadas células T citotóxicas, linfocitos exterminadores del agente invasor. Asimismo, es capaz de identificar y eliminar células tumorales; estas células que han mutado expresan antígenos específicos (unas proteínas) que el sistema inmune reconoce como extraños-malignos, activándose la respuesta inmunitaria. Todo apunta a que a lo largo de nuestra vida y sin que nos demos cuenta, el sistema inmune se encarga de neutralizar estas mutaciones celulares evitando la aparición de muchos más tumores.
Sin embargo, algunos tipos de células cancerígenas tienen estrategias para escapar de las células inmunitarias: son capaces de expresar en su superficie una serie de proteínas (puntos de control) que hacen que los linfocitos queden adormecidos, frenados en su actividad. Entre estas proteínas adormecedoras destaca PD1 (y su oponente PDL1), y se hallan en las células T inmunitarias para regular la intensidad de su acción, de modo que no ataquen células sanas o células tumorales que expresan PDL1.Existen otras moléculas 'adormecedoras' que reducen la respuesta inmunitaria, entre las que destaca la denominada CTLA4. Los tratamientos que consiguen despertar estas células para que ataquen las células cancerosas son los anticuerpos monoclonales, que se unen a estas proteínas y desactivan ese freno. Así, los medicamentos con anticuerpos monoclonales aprovechan las funciones del sistema inmunitario natural para combatir el cáncer, y pueden utilizarse en combinación con otros tratamientos oncológicos y también con otras inmunoterapias; de hecho, se ha constatado que es precisamente con la combinación de tratamientos inmunoterápicos cuando se obtienen mayores éxitos. Algunos de los anticuerpos monoclonales inhibidores de puntos de control inmunológico son el ipilimumab, para la diana terapéutica CTLA4, el pembrolizumab y el nivolumab para la diana terapéutica PD1, y atezolizumab, avelumab o durvalumab para la PD-L1.
Otro inmunotratamiento es la terapia celular adoptiva; y de entre ellas destaca la terapia de células T con CAR, que se basa en extraer linfocitos T de la sangre, activarlos y modificarlos genéticamente para que expresen el receptor CAR mediante manipulación o ingeniería genética se les ha conferido la capacidad de reconocer y destruir las células tumorales, expandir estas células en el laboratorio y volver a transfundirlas al paciente.
La terapia con virus oncolíticos viroterapia, por su parte, utiliza virus modificados genéticamente para que infecten sólo las células cancerígenas; una vez inyectados directamente en el tumor, estos destruyen las células tumorales provocando la liberación de antígenos tumorales que ayudan al sistema inmune a reconocer estas células, donde quiera que se encuentren, y entrar en acción.
En el capítulo de las vacunas terapéuticas, mediante biotecnología se identifican antígenos específicos de cada tumor para que, una vez producidos in vivo o ex vivo, causen una respuesta inmunitaria al antígeno en cuestión, que destruya las células cancerosas o bien detenga o retrase su crecimiento. Y es que una circunstancia a tener en cuenta en inmunoterapia, que no se da con la quimioterapia, es la posibilidad de alcanzar un equilibrio que permita a un paciente convivir con un tumor sin que éste progrese. Así lo explica el doctor Manel Juan: En inmunoterapia se da lo que vendrían a ser tres fases reales: cuando vemos que hay un tumor y que está creciendo es que el sistema inmunitario no está funcionando, entonces decimos que es un mecanismo de escape el tumor está creciendo porque se escapa al bloqueo del sistema inmune, y como contrapartida para curarlo, lo que buscamos es llegar a la fase de eliminación que el sistema inmune elimine el tumor; pero entre el escape y la eliminación hay una situación de equilibrio en la que los tumores pueden no crecer durante mucho tiempo. Lo hemos visto en pacientes que no tenían otra opción y después de tratarse con inmunoterapia, el tumor no ha progresado durante un largo período.
¿Por qué ahora?
La investigación en inmunoterapia ha permanecido bloqueada durante muchos años, coincidiendo con el desarrollo de la radioterapia y la quimioterapia, pero ¿qué circunstancias han cambiado para que se haya retomado el sistema inmunológico como objeto de estudio? Hoy argumenta la doctora Garralda se une un conocimiento que ya había sobre que el sistema inmune puede atacar tumores, un mayor conocimiento de la capacidad del tumor de evadir el sistema inmune, que es una de las capacidades que adquiere en su propia deriva y evolución tumoral, y que empiezan a aparecer fármacos que incluso en monoterapia pueden tener una respuesta efectiva muy duradera. Hay pacientes con tumores metastásicos que llevan 10 años libres de enfermedad, y eso son resultados que con otras terapias no veíamos; de ahí que haya un crecimiento espectacular del interés por investigar este tipo de moléculas.
En opinión de Manel Juan: Se ha tardado porque, básicamente, había un claro interés en el desarrollo de productos químicos con efecto directo contra el tumor, ya que con las quimioterapias el efecto se centraba en el tumor, y el procedimiento quimioterápico ha dado mucho margen para ello; incluso después del conocimiento de las mutaciones, las investigaciones también se han centrado en inhibidores de funciones concretas de las células mutadas a nivel químico.
El despegue de estas terapias coincide con el estancamiento de las posibilidades de la quimioterapia, que después de alcanzar un nivel de éxito muy importante, ha visto como en los últimos años, los fármacos que han ido apareciendo no han aportado cambios sustanciales; mientras que la inmunoterapia, con su cambio de concepto, ofrece la posibilidad de tratar también un cáncer, pero, generalmente, con muchos menos efectos secundarios. En este sentido, la valoración de nuestro interlocutor es que el interés por la producción de moléculas que actúan sobre la biología ha llegado cuando la química ya no daba mucho más de sí. Hoy las farmacéuticas ven que las terapias biológicas aportan nuevas opciones.
Uno de los factores que ha retrasado el desarrollo de la inmunoterapia fue, en su momento, la irrupción de la quimioterapia, que ha ido en gran parte en contra de las opciones de inmunoterapia: administrar un tóxico directamente contra el tumor, también suele ser tóxico para el sistema inmunitario, recuerda Juan. Aunque existen distintas quimioterapias y pautas de tratamiento en función, entre otros factores, de la fase tumoral, el caso es que con quimioterapia se consiguen respuestas rápidas y relevantes (mayoritariamente por encima del 20%), y eso prosigue Juan es más fácil de entender que esperar un reequilibrio de la función del sistema inmunitario, que lleva un cierto tiempo. Aplicar una radiación o una quimioterapia que mate es más claro de entender desde el punto de vista de opción terapéutica. La inmunoterapia no suele ser tan rápida; se necesita un cierto tiempo para que el sistema inmunitario funcione.
Otra circunstancia que ha contribuido al impulso de estas terapias ha venido de la mano de los fármacos monoclonales, que han cambiado el criterio de evaluación de las respuestas. Así lo explica el doctor Juan: Con la llegada de estos fármacos la industria ha conseguido cambiar los criterios de evaluación oncológica que se usan en la valoración de las agencias del medicamento; hasta entonces, a menudo ocurría que la inflamación que se produce al atacar con el sistema inmunitario el tumor hace que parezca que éste crezca (pseudoprogresión), y ante esta situación, de manera comprensible, el criterio de quienes no valoran bien el sistema inmunológico hacía descartar esta opción sin dar tiempo a comprobar si funcionaba en el paciente en realidad, es positivo que haya inflamación porque eso significa que está funcionando. Ahora se entiende que se necesita más tiempo para ver si después de la inflamación hay una mejora; este hecho ha sido definitivo. En todo caso, habrá que ver cómo se implementa, en qué casos se aplicará antes de una quimioterapia, en quiénes funcionará o no, etc.; especialmente porque, por ahora, las inmunoterapias disponibles son tratamientos de alto coste. Este objetivo pasa por identificar biomarcadores que ayuden en la predicción de quién responderá a la inmunoterapia, y a ello contribuirán nuevas pruebas como los test genómicos o la biopsia líquida.
También la microbiota de nuestro sistema digestivo puede constituir un indicador de en qué pacientes es más probable que funcione un fármaco de inmunoterapia. Recientes investigaciones demuestran que la respuesta a una inmunoterapia depende de esa población bacteriana. En sentido contrario, aunque complementario, el ámbito de la inmunoterapia (en este caso con objetivo antiinfeccioso) también puede dar respuesta al reto acuciante de combatir la resistencia antibiótica.
Entre las cuestiones que quedan por determinar se encontrarían los posibles efectos adversos de estas nuevas terapias que, aunque suelen ser menores que los que genera la quimioterapia, deberán ser previstos y/o controlados de manera más efectiva.

Producción inmunoterápica
¿Es la inmunoterapia un medicamento? Pues aunque existen algunas discrepancias entre la comunidad científica respecto a considerar estas terapias un medicamento, como argumenta Manel Juan, en el momento en que extraes células y las manipulas, incluso con las células del propio paciente que es distinto a utilizar un producto externo, eso ya es un fármaco. La normativa, tanto en EE.UU. como en Europa, así lo determina y ello conlleva los mismos criterios de calidad y de control que un producto farmacéutico; podía haber sido considerado trasplante, que tiene otra regulación, pero no se ha conseguido que esto fuera así.
A este respecto cabe mencionar dos niveles de tratamiento inmunoterápico. Por una parte, se encuentran los productos provenientes y producidos fuera del individuo al cien por cien detalla el doctor; al paciente se le introduce un producto externo, por ejemplo, anticuerpos monoclonales como el citado anti-PDL1, que trata de regular el sistema inmune. Por otro lado, tenemos aquellos tratamientos en los que manipulas sus propias células (aunque lo hagas fuera del individuo), ya sea para generar respuesta (por ejemplo, con las vacunas terapéuticas con células dendríticas), o bien cogiendo los linfocitos antitumorales y manipulándolos para que puedan eliminar el tumor. En este sentido, Manel Juan propone una reflexión sobre la materia prima de estas terapias, que sugiere un cambio de concepto: Pensemos que el paciente también le da algo a la industria ya que ésta se beneficia de un producto que no es propiamente suyo, puesto que proviene del mismo paciente y la industria solo modifica lo que se le presta.
Nuestro interlocutor considera que el hecho de que las inmunoterapias estén estructuradas como fármaco (hace más de 10 años que tienen esta consideración) constituye un condicionante para su aplicación masiva a corto plazo ya que los fármacos apunta necesitan, para ser aprobados, unos niveles de inversión muy altos; si cambiara la normativa y se consiguiese que fuesen equivalentes al trasplante, se facilitaría su introducción. Que sean fármacos hace que necesites muchísima inversión económica, se requieren ensayos clínicos de alto nivel de inversión que, prácticamente, solo pueden realizar las grandes industrias farmacéuticas.
Los descubrimientos no cesan. La EMA aprobó el año pasado 84 medicamentos, de los que la mitad son nuevas moléculas y entre los nuevos fármacos se incluyen tres nuevas terapias génicas y celulares, dos de ellas basadas en las CAR-T.
La pregunta ahora es cuándo la población podrá beneficiarse masivamente de estos nuevos hallazgos. En opinión de Manel Juan con respecto a los altos costes de estas terapias, su implantación depende de cómo se estructure, pero, rotundamente, sí es posible llegar a masificar las inmunoterapias; hay capacidad para poder hacerlo.
































