La medida del potencial de oxígeno en los procesos de tratamientos térmicos de los metales
1 de diciembre de 2008
El diagrama de la figura 1 muestra esta característica para diversos elementos. El níquel por ejemplo, se oxidará para convertirse en NiO en una atmósfera con un potencial superior a -60 kilocalorías/mol a 1000 °C o -81 kilocalorías/mol a 500 °C. El cromo tiene una mayor afinidad con el oxígeno que el níquel como indica la línea inferior del diagrama. Requeriría un potencial de oxígeno inferior a 130 kilocalorías/mol a 1000 °C para evitar la oxidación. Por tanto, una atmósfera adecuada para evitar la oxidación del níquel no evitaría la oxidación del cromo. Las líneas del diagrama son para el estado de oxidación más bajo del elemento.
Este tipo de diagramas permiten determinar el nivel teórico del potencial de oxígeno para una variedad de condiciones. Por ejemplo, si se desea decarburar el acero mediante la oxidación de parte del carbono en el metal, pero al mismo tiempo se quiere evitar la oxidación del metal a 1000 °C, se podría lograr con un potencial de oxígeno de -100 kilocalorías/mol. Por debajo de los 750 °C no sería posible decarburar sin oxidar el hierro del acero dado que la línea de carbono cruza la línea de hierro en el diagrama de la energía libre a esta temperatura.
En el pasado, la medida de la capacidad de oxidación/reducción de una atmósfera protectora, o del potencial de carbono de una atmósfera carburante, se conseguía por deducción o bien midiendo el contenido de CO2, o bien mediante el ratio CO/CO2 o bien mediante el punto de rocío (el contenido de humedad), según la naturaleza de la atmósfera. Sin embargo, estas medidas se pueden relacionar directamente al potencial de oxígeno o a la presión parcial de oxígeno. Por ejemplo, un gas exotérmico rico con un ratio de CO/CO2 de 10 tiene un potencial de oxígeno de -93 kilocalorías/mol o una presión parcial del oxígeno de 10-16 atmósferas a 1000 °C. En cambio, un gas exotérmico pobre con un ratio de CO/CO2 de 0,1 tiene un potencial de oxígeno de -70 kilocalorías/mol o una presión parcial del oxígeno de 10-12 atmósferas a 1000 °C. El amoniaco craqueado, que se usa a menudo para el temple del acero inoxidable, se monitoriza mediante la medida del punto de rocío. Esto se relaciona con el contenido de agua en el gas del cual se extrae el ratio H2/H2O (asumiendo que el contenido de H2 es conocido y constante) que a su vez se relaciona con el potencial de oxígeno.
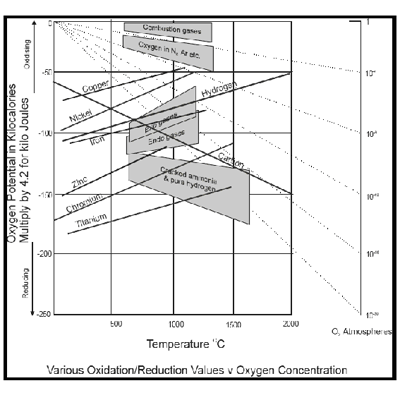
Estos datos sólo dan información sobre si un metal se oxidará o no en ciertas condiciones; no dice nada sobre el ratio de oxidación, etc. Factores como éstos supondrán que se pueden permitir potenciales de oxígeno más elevados de los que las consideraciones teóricas por sí solas indicarían. Además, en algunos casos, una cierta oxidación de la superficie del metal puede ser aceptable. Se deberían tomar en consideración factores como éstos a la hora de determinar la forma más económica de llevar a cabo un proceso. Un analizador de oxígeno con célula de circonio puede suministrar información muy valiosa para analizar el efecto de varias condiciones, así como controlar la condición óptima una vez ésta se haya establecido.
Atmósferas
Las atmósferas exotérmicas se producen con la quema de un combustible gaseoso, típicamente gas natural o metano, en cantidades variables de aire. Estas atmósferas pueden variar mucho según la composición del ratio aire/gas. Comúnmente se las denomina atmósferas ricas o pobres. Las atmósferas ricas contienen demasiado combustible que a veces supone que son inflamables ellas mismas, mientras que las atmósferas pobres no. La atmósfera se utiliza para proteger los metales de la oxidación durante los procesos de tratamiento térmico como el temple. Las atmósferas ricas tienden a utilizarse con metales férricos que requieren un contenido de oxígeno más bajo que los metales no-férricos, que tienden a utilizar atmósferas pobres para protegerlos.
A veces se tratan las atmósferas exotérmicas para retirar agua y/o dióxido de carbono. Una vez más, éstas varían mucho en su composición según el gas inicial y el tratamiento que se le realice. A menudo contienen grandes cantidades de hidrógeno que se puede utilizar como medida de la calidad del gas junto con el potencial de oxígeno.

El amoniaco craqueado se produce con la descomposición del amoniaco (NH3) en hidrógeno y nitrógeno. Es una forma práctica de producir hidrógeno y el proceso se puede controlar midiendo el contenido de hidrógeno. En ocasiones se requiere el valor en porcentaje de disociación que el analizador K1550 de Hitech puede suministrar.
El amoniaco quemado se produce simplemente haciendo esto, quemando amoniaco, normalmente en presencia de un catalizador. Se genera una atmósfera de hidrógeno, nitrógeno y agua, y a menudo se seca un poco mediante evaporación del amoniaco para enfriar el gas. Una vez más, la monitorización del contenido de hidrógeno es muy importante.
Los procesos que utilizan estos gases son principalmente de tres tipos:
Recocido: cuando se calienta un metal para ablandarlo antes de realizarle otros procesos como laminado o conformado. Según la atmósfera, será útil monitorizar el oxígeno, el hidrógeno o ambos.
Carburación: cuando se hace reaccionar la superficie de los metales ferrosos con carbono para crear una capa exterior de metal más duro. Hoy en día para esta aplicación se acostumbra a utilizar una sonda de oxígeno in-situ. La desventaja de utilizar un sistema exsitu sería que en atmósferas muy ricas se produciría hollín. El sistema exsitu de bajo coste puede utilizarse en procesos de ciclo largo con atmósferas en las que no se suele producir tanto hollín.
Tratamiento superficial cosmético: procesos como el azulado y el recocido brillante del acero. El azulado se realiza a menudo en atmósferas húmedas (de hecho en ocasiones se utiliza vapor) por lo que será necesario aislar bien el sensor para evitar condensaciones. El analizador de Hitech Z1900 es ideal para este tipo de procesos.
Factores de conversión:
1) Kilo Joule (kJ) = kilocaloría (kcal) x 4.187
2) * kJ = (17.6 x log % oxígeno) 34.72
* Sólo aplicable a analizadores de oxígeno de Hitech que operan a 45mV por década (634°C).






