Aidimme obtiene fotocatalizadores nanoestructurados y superficies poliméricas activadas bactericidas
El proyecto Filtair, desarrollado por el Instituto Tecnológico Aidimme, ha obtenido fotocatalizadores nanoestructurados de TiO2 y superficies poliméricas activadas de PP y PU con rendimientos de eliminación de virus y bacterias cercanos al 100%. Esto ha sido posible mediante la combinación de tecnologías de fabricación aditiva y técnicas electroquímicas de modificación superficial.
A raíz de la aparición del virus SARS-CoV-2 la sociedad se siente más vulnerable y demanda una mayor protección frente a patógenos en distintos entornos, tanto sanitarios como en otros más cotidianos como el laboral, entretenimiento o hábitat. El control y limpieza del aire que respiramos o de las superficies que nos rodean está conduciendo al desarrollo de soluciones tecnológicas hasta ahora no planteadas. En este sentido la nanotecnología está jugando un rol relevante, sobre todo por su potencial para la funcionalización superficial.
Por otra parte, la fabricación aditiva para la fabricación de piezas a partir de un modelo 3D, para materiales tan dispares como el metal, plástico o cerámica, se está posicionando como tecnología de fabricación de alto valor añadido. Su elevada rapidez, versatilidad geométrica y de diseño, el ahorro de material o la personalización del producto final son algunas ventajas frente a los sistemas de fabricación convencional. Además, presenta una estructura superficial única debido a su proceso de fabricación, generando microestructuras que pueden mejorar sus prestaciones en sistemas electroquímicos.
Protección microbiana, nanotecnología y fabricación aditiva son los tres ejes sobre los que el proyecto Filtair ha trabajado con objeto de aportar soluciones tecnológicas para la creación de entornos más seguros. Los desarrollos realizados han sido la creación de superficies bactericidas a través de la creación de fotocatalizadores nanoestructurados de TiO2 y la funcionalización química de materiales poliméricos de polipropileno y poliuretano.
Fotocatalizadores nanoestructurados de TiO2
Sustrato y tecnología de fabricación
Entre todas las aleaciones de titanio se escogió la aleación Ti6Al4V para la creación de fotocatalizadores de TiO2 ya que es la que más destaca en su uso dentro de la fabricación aditiva, fundamentalmente gracias a sus excelentes propiedades mecánicas, resistencia a la corrosión, ligereza y biocompatibilidad [1]. El sector salud [2, 3] es donde más se aplica, utilizándose también en sectores de alto nivel tecnológico y prestaciones como el aeronáutico, aeroespacial o marino.
En este trabajo se han estudiado como afectan distintos tratamientos electroquímicos y térmicos sobre dos superficies de titanio procesado por tecnologías de fabricación aditiva (Ti6Al4V-FA) con tecnología de fusión de lecho de polvo. Una fabricada con tecnología Láser, PBF-LB, - y otra fabricada con tecnología por haz de electrones, PBF-EB. Ambas tecnologías se compararon con barras de titanio comercial para comprobar el efecto de la FA en los procesos de modificación superficial estudiados para la aplicación de fotocatálisis antibacteriana. Para ello, se fabricaron distintas tipologías de probetas, tanto macizas como en formato rejilla, figura 1, con el objetivo de estudiar las distintas superficies obtenidas según el método de fabricación y su estructura. Dichas probetas se realizaron en formato piruleta en las que la superficie a modificar era de 1 cm2 con una conexión eléctrica de 1,5 cm.

Modificación superficial
Para conseguir una modificación superficial del titanio nanoestructurada se ha utilizado una combinación de técnicas electroquímicas-térmicas basadas en el anodizado. El sistema consiste en una oxidación controlada de la superficie, creando una nanoestructura de óxido del material base como resultado del movimiento del campo eléctrico aplicado [4]. El anodizado le confiere a la superficie propiedades funcionales únicas, aumentando sus prestaciones en sectores en los que puede ser de interés el Ti6Al4V-FA, como son el de sensores [5], baterías de ión-litio [6], generación de hidrógeno [7], celdas solares [8], degradación de contaminantes por fotoelectrocatálisis y electrocatálisis [9, 10], así como en la aplicación bactericida objetivo [11].
La modificación superficial controlada mediante anodizado permite obtener una elevada área superficial de contacto, aumentando las propiedades de transporte electrónico, y con ello su capacidad fotocatalítica. En el caso concreto del proyecto Filtair la consecuencia es la generación de un elevado efecto bactericida
Se consiguió la creación de superficies nanoestructuradas utilizando dos rutas distintas de anodizado electroquímico, una a potencial constante y otra a potencial pulsado, terminando en ambos casos con un tratamiento térmico de oxidación-reducción. En la figura 2 se muestra a modo de ejemplo algunas de las estructuras que se consiguieron obtener sobre la superficie del Ti6Al4V-FA fabricado por PBF-LB.

Figura 2. Diferentes micrografías obtenidas en muestras de fabricación aditiva por PBF-LB en función del tratamiento superficial realizado.
Se ha podido comprobar, que cada técnica utilizada, modifica las superficies iniciales de forma distinta, consiguiendo tras su optimización poder controlar la estructura formada en cada caso. Además, dicha modificación superficial, se corresponde a una morfología y respuesta fotocatalítica diferente.
En este trabajo de investigación, se muestran, a modo de ejemplo, solamente los resultados obtenidos tanto en la respuesta fotocatalítica como la evaluación antimicrobiana del tratamiento realizado mediante potencial pulsado, utilizando una luz cercana al visible de λ=405 nm como fuente de energía.
Respuesta fotocatalítica
Las propiedades fotocatalíticas de las muestras preparadas fueron evaluadas con medidas fotoelectroquímicas. En ellas, se comparó el incremento de corriente asociado a la generación fotoelectrocatalítica de TiO2 alternando condiciones de luz y oscuridad.
En todos los casos, tanto en las muestras fabricadas por PBF-EB y PBF-LB como en la barra comercial, se ha comprobado que el proceso de anodizada mejora la respuesta fotoelectroquímica a una longitud de onda dada, obteniéndose valores mayores de corriente en todo el rango de potencial estudiado, como puede verse a modo de ejemplo en las imágenes a, c y e) de la figura 3, para el caso particular de anodizado por onda pulsante.
Además, las imágenes b, d y f) de la figura 3, muestran de forma comparativa, a un mismo potencial de trabajo y longitud de onda, alternando condiciones de luz y oscuridad, como los materiales de FA aumentan la fotocorriente obtenida respecto a la barra comercial, siendo mayor ésta diferencia en las muestras anodizadas. Así, las muestras que registran mayores valores de fotocorriente siguen el siguiente orden: PBF-LB>PBF-EB>Barra comercial. Por lo tanto, hay un efecto claro en el modo de fabricación sobre la respuesta fotocatalítica.
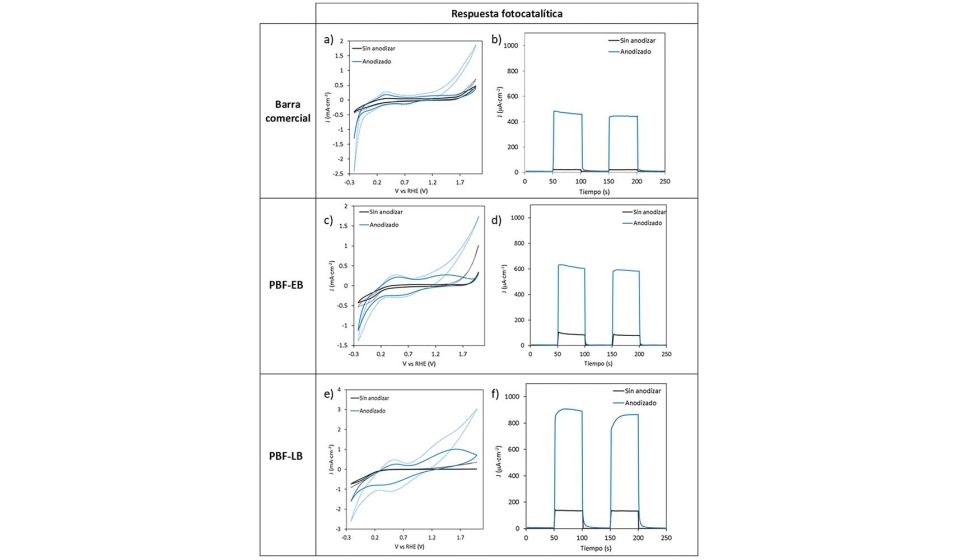
Figura 3. Imágenes a, c y d) Curvas de voltametría cíclica de las tres muestras estudiadas sin anodizar y anodizadas por onda pulsante. Las líneas punteadas se refieren a la respuesta del sistema con luz de λ=405 nm, mientras que las líneas sólidas son los datos obtenidos en oscuridad. Imágenes b, d y f) Curvas a potencial constante (1,6 V vs RHE) de las tres muestras anodizadas mediante onda pulsante con y sin estímulo de luz a λ=405 nm.
Evaluación fotocatalítica antimicrobiana
La efectividad de las modificaciones superficiales sobre el efecto fotocatalítico antimicrobiano se realizó según la norma ISO 27447:2019, que evalúa la actividad antibacteriana en materiales fotocatalíticos. La bacteria utilizada fue Escherichia coli mediante la generación de un pseudobiofilm sobre la superficie de las muestras durante 15 minutos con y sin exposición de luz. La evaluación antimicrobiana se llevó a cabo mediante la determinación de la reducción logarítmica de la suspensión de células bacterianas puestas en contacto sobre la superficie de ensayo, tras un determinado tiempo de incubación, cuya expresión viene expresada a continuación.
?R=log (BL/CL)-log (BD/CD)
Donde:
?R Es la actividad antibacteriana fotocatalítica con irradiación UV.
BL Es la media del número viable de bacteria de muestras no tratadas tras la irradiación UV.
CL Es la media del número viable de bacteria de muestras tratadas tras la irradiación UV.
BD Es la media del número viable de bacteria de muestras no tratadas tras la incubación en oscuridad.
CD Es la media del número viable de bacteria de muestras tratadas tras la incubación en oscuridad.
En la figura 4 aparecen los resultados de dicha evaluación sobre la barra comercial y las piezas fabricadas por PBF-LB anodizadas mediante potencial pulsado y ensayadas sin y con la luz de λ=405 nm.
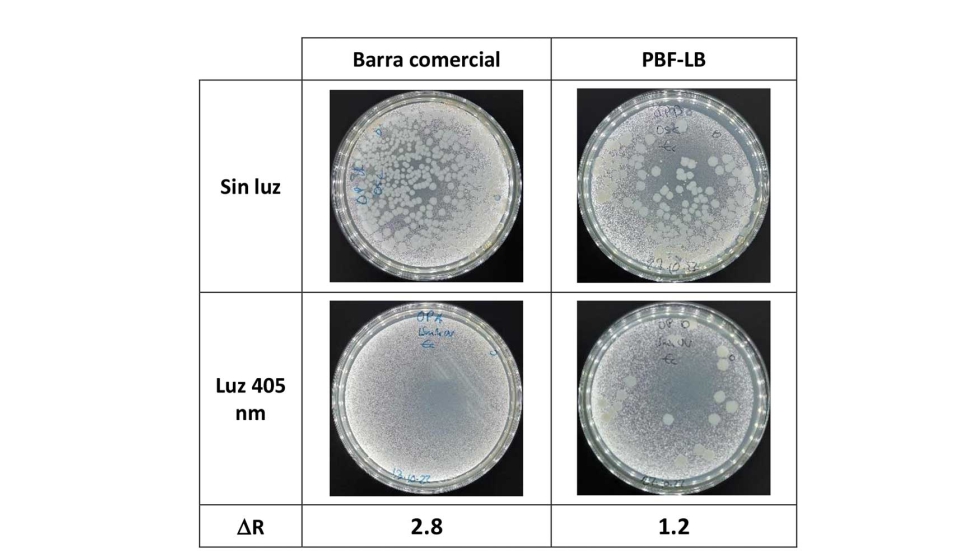
Figura 4. Imágenes de los ensayos antimicrobianos de los lavados sin dilución de la barra comercial y de las muestras de fabricación aditiva por PBF-LB, ambas anodizadas mediante onda pulsante con y sin estímulo de luz a λ=405 nm y valores de la actividad antibacteriana fotocatalítica para ambas muestras.
Los resultados de actividad fotocatalítica antibacteriana muestran efectividad tanto en la barra como en la muestra fabricada mediante fabricación aditiva. Además, también se observa como existe un efecto antimicrobiano no fotocatalítico debido al proceso de fabricación, ya que existe una disminución clara de las colonias de E. coli en la muestra fabricada por PBF-LB respecto a la barra comercial.
De esta manera, se ha demostrado que el proceso de fabricación aditiva mejora la actividad antimicrobiana de superficies modificadas mediante anodizado por onda pulsante. Además, también se demuestra que las superficies obtenidas mediante el tratamiento de potencial pulsado tienen un efecto fotocatalítico claro, tanto en la barra como en la pieza de fabricación aditiva, siendo ligeramente mayor en el de barra frente al de FA.
Funcionalización de superficies poliméricas de PP y PU
Sustratos y tecnologías de fabricación
Se ha trabajado con polipropileno y poliuretano como materiales poliméricos, utilizando en ambos casos tecnologías 3D para su fabricación.
Se ha seleccionado el polipropileno (PP) por ser uno de los materiales más versátiles, debido a su bajo coste, por ser inerte químicamente y por sus buenas propiedades mecánicas. Sin embargo, su naturaleza hidrofóbica restringe su aplicación en una serie de áreas tecnológicamente importantes haciendo necesario su modificación superficial para funcionalizarlo mediante técnicas de activación mediante plasma u ozono.
Por otra parte, también se estudió el poliuretano (PU), por ser uno de los materiales más utilizados en biomateriales principalmente en el sector médico, recubrimientos y adhesivos debido a sus excelentes propiedades mecánicas, resistencia a la abrasión, durabilidad, flexibilidad, bajo peso y por su biocompatibilidad [12]. Sin embargo, su alta hidrofobicidad y la facilidad de proliferación de las bacterias sobre su superficie hacen que sea necesaria su modificación superficial para evitarlo [13].
Para fabricar los sustratos de polipropileno se ha empleado la tecnología de lecho de polvo de polímeros, comúnmente conocida como Multi Jet Fusion (MJF) con una impresora 3D de HP 5200. Esta tecnología utiliza materiales termoplásticos en forma de polvo fino para crear piezas en tres dimensiones. Y en el caso del poliuretano se ha utilizado la tecnología de fotopolimerización en tanque con curado por exposición a luces de diodos emisores de luz, VPP-LED, en concreto la tecnología 3D Liquid Crystal Display, figura 5. Ésta trabaja con resinas fotosensibles que se curan capa a capa de forma invertida creando piezas en tres dimensiones. La fuente de curado está formada por un panel LCD de alta resolución y de longitud de onda en torno a los 405 nm.

Figura 5. Imágenes de las piezas de PP y PU utilizadas y del proceso de fabricación de las piezas de PU mediante tecnología VPP-LED.
Bactericida por contacto
Las superficies bactericidas pueden actuar mediante tres mecanismos: repulsión, liberación de agente bactericida y contacto. De los tres sistemas se ha seleccionado el de contacto por sus ventajas más destacables: larga duración, no liberar productos químicos y matar al patógeno.
La incorporación de componentes de amonio cuaternario con silanos es una de las vías más prometedoras para sistemas de desinfección por contacto sobre superficies, fundamentalmente por su fácil incorporación, compatibilidad, durabilidad, eficacia y seguridad [14]. En este sentido, se ha seleccionado un agente bactericida por contacto de silano de amonio cuaternario, SiQAc, con una cadena C-18. El mecanismo bactericida es por atracción y rotura de las enzimas y membrana celular de las bacterias [15]. Las bacterias quedan adheridas e inmovilizadas a la molécula que actúa como una espada rompiendo su pared celular.
El reto de la técnica de funcionalización de superficies por bactericidas por contacto es realizar un enlace fuerte entre las superficies y los compuestos de silano de amonio cuaternario para evitar su migración y que queden formando parte de su superficie, modificándola y funcionalizándola. Este enlace consigue que el agente bactericida este contenido en el sustrato original sin que se pierda con el tiempo, como es el caso de los bactericidas por liberación.
Modificación superficial
La modificación superficial se ha llevado a cabo a través de dos metodologías:
- Funcionalización directa por enlace covalente previa activación superficial.
- Recubrimiento sol-gel que contenga al agente bactericida.
En el caso de la funcionalización directa se lleva a cabo una activación previa de la superficie, generando grupos -OH. Para ello se han aplicado la tecnología de plasma atmosférico y la radicación UV de 254 nm.
En los dos métodos estudiados, las tecnologías de aplicación utilizadas han sido las siguientes: dip-coating (DC), esprayado (SC), esprayado con ultrasonidos (US-SC) y Casting La que mejores resultados ha obtenido fue la técnica de inmersión o dip-coating (DC) en una disolución o recubrimiento con el agente bactericida con posterior tratamiento térmico de secado. De esta forma se consigue fijar el SiQAc en la superficie de forma eficaz. Además de fijar el amonio cuaternario se ha comprobado si incorporando Ag a la disolución o recubrimiento de aplicación existía un efecto sinérgico.
Para comprobar el anclaje del SiQAc sobre las superficies se realizaron caracterizaciones tanto visuales, a través de colorantes como el azul de bromofenol, como estructurales mediante espectroscopía de infrarrojos, FTIR.
En la figura 6 se muestran, a modo de ejemplo, algunas de las piezas de poliuretano tras la funcionalización por anclaje directo tras su activación, utilizando varios métodos de aplicación. En concreto, se pueden ver los resultados de la prueba por aplicación por Spray Ultrasónico (US-SC) con varias pasadas de la boquilla de esprayado (a-d), aplicación mediante inmersión en disolución (DC) de SiQAc durante 24 horas (e-f) y su comparación con una superficie de poliuretano sin realizar el anclaje tras el paso del colorante (g). De la imagen, se puede extraer que las muestras más coloreadas son las que la funcionalización se aplica mediante DC-24h. Además, se observa que las piezas que no se les ha aplicado el agente bactericida no se colorean, por lo que el método del azul de bromofenol es válido para detectar si el compuesto SiQAc se encuentra anclado sobre la superficie de las piezas.
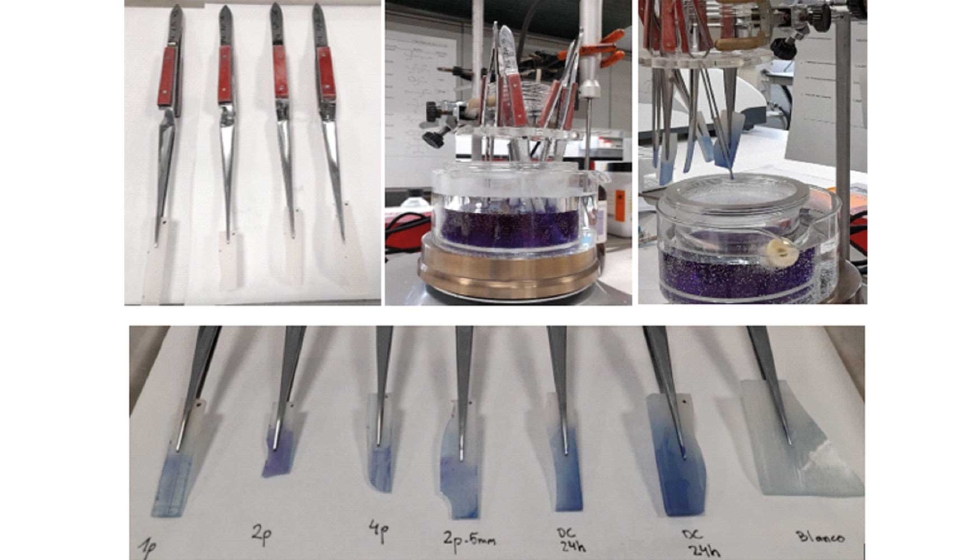
Figura 6. En las imágenes superiores se muestra el proceso de comprobación visual del colorante tras aplicar el SiQAc sobre superficies de PU. En la imagen inferior de izquierda a derecha se muestran los resultados de los siguientes métodos de funcionalización por a) US-SC 1pasada; b) US-SC 2 pasadas; c) US-SC 4 pasadas; d) US-SC 2p-5mm; e y f)DC 24h; g) superficie sin funcionalizar, blanco.
En el caso de las caracterizaciones mediante espectroscopía de infrarrojos, digura 6, también se pudo comprobar la existencia del SiQAc sobre las muestras funcionalizadas mediante activación y anclaje por DC, imágenes figura 7a para el PP y Figura 7b para el PU. En el caso del método de recubrimiento sol-gel, también se pudo ver claramente como el agente bactericida SiQAc se encontraba integrado en el recubrimiento, tanto por sí solo como formando parte de un recubrimiento híbrido con plata, figura 7c, los picos característicos del SiQAc a longitudes de onda a 3.300 cm-1 se observan en todos los espectros, así como las bandas características de los enlaces de silano, Si-O-Si en valores de 1.100 cm-1.
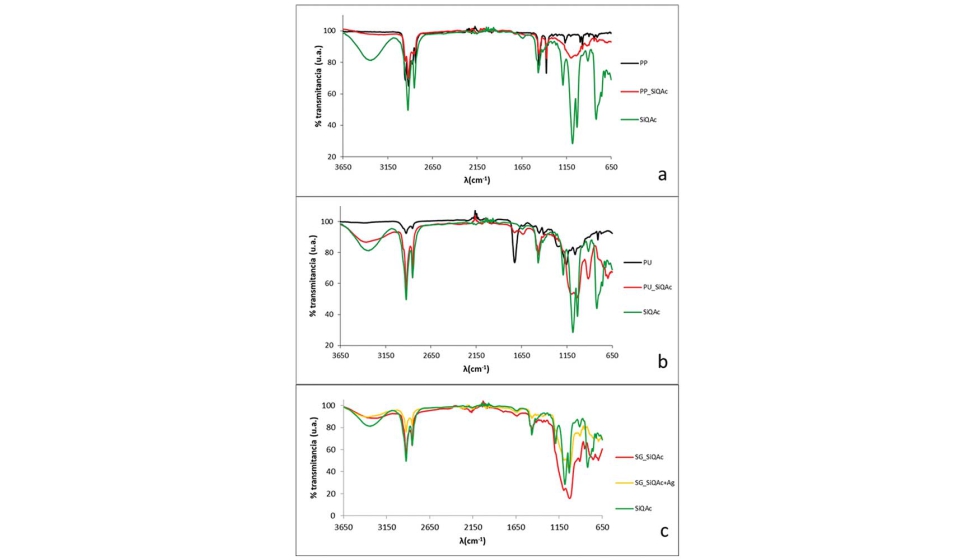
Figura 7. Espectros de infrarrojos de las superficies de a) PP y b) PU tras su funcionalización por activación y anclaje directo sin y con SiQAc y su comparación con el agente bactericida como reactivo; c) espectros de infrarrojos de los recubrimientos sol-gel funcionalizados con SiQAc y SiQAc+Ag y su comparación con el agente bactericida como reactivo.
Tras las modificaciones superficiales sobre el PP y PU se puede comprobar, que su aspecto en ambas estrategias, no se ve alterado, es uniforme y homogéneo en todos los casos, menos en el de PU por sol-gel dónde sí que se observa un brillo sobre la superficie, figura 8.
Por lo tanto, se ha podido funcionalizar correctamente ambos materiales, el PP y el PU, fabricados mediante tecnologías de fabricación aditiva, con un bactericida de contacto de amonio cuaternario, el SiQAc, sin prácticamente alterar su superficie.

Figura 8. Imágenes de los sustratos poliméricos tras su funcionalización con recubrimiento sol-gel y de los recubrimientos sin sustrato tras el proceso de secado.
Evaluación antimicrobiana
Tras la optimización de la metodología de ambas estrategias se consiguieron superficies funcionalizadas con el SiQAc en las que se evalúo su efecto bactericida utilizando la bacteria Escherichia coli como control. Se ensayaron las muestras de Polipropileno y Poliuretano, en cabina de flujo laminar, conforme a la metodología utilizada en la norma ISO 22196: 2011 Measurement of antibacterial activity on plastics and other non-porous surfaces.
La evaluación se realizó tras un periodo de incubación de las placas de 24 horas, a 35 °C y 90% de humedad relativa, con una concentración inicial de bacterias E. coli de 5·105 UFC/mL. Los resultados se compararon con los obtenidos de los ensayos realizados en las mismas condiciones sobre las piezas de control. En el caso de la estrategia de activación + anclaje directo, el control fue el sustrato original sin tratamiento y en el caso de la estrategia de modificación de recubrimiento, el control fue un sustrato recubierto con el sol-gel sin agente bactericida.
En la figura 9 se pueden ver los resultados de dicha evaluación. En la imagen de la izquierda se muestra los resultados para la modificación superficial con recubrimiento sol-gel. El control es un recubrimiento sin agentes bactericidas. Dicho control se compara con tres muestras en las que se han incorporado dos agentes bactericidas, la plata y el SiQAc por separado y en último lugar conjuntamente. En la imagen superior derecha, se muestran los resultados en la modificación superficial mediante activación+ anclaje. Finalmente, en la tabla situada en el margen derecho inferior de la figura, se muestran los valores cuantitativos de todas las muestras tras la evaluación antimicrobiana.
Como se puede ver, existe un claro efecto bactericida en ambas estrategias para ambas técnicas, llegando a valores cercanos al 100% de eliminación. El único que no presenta efecto bactericida es el caso del anclaje directo del PU. También se observa que el efecto del SiQAc por sí solo es suficiente para generar un efecto bactericida claro sobre ambas superficies en los recubrimientos sol-gel y que es comparable al efecto de un bactericida por liberación como es el caso de la plata.
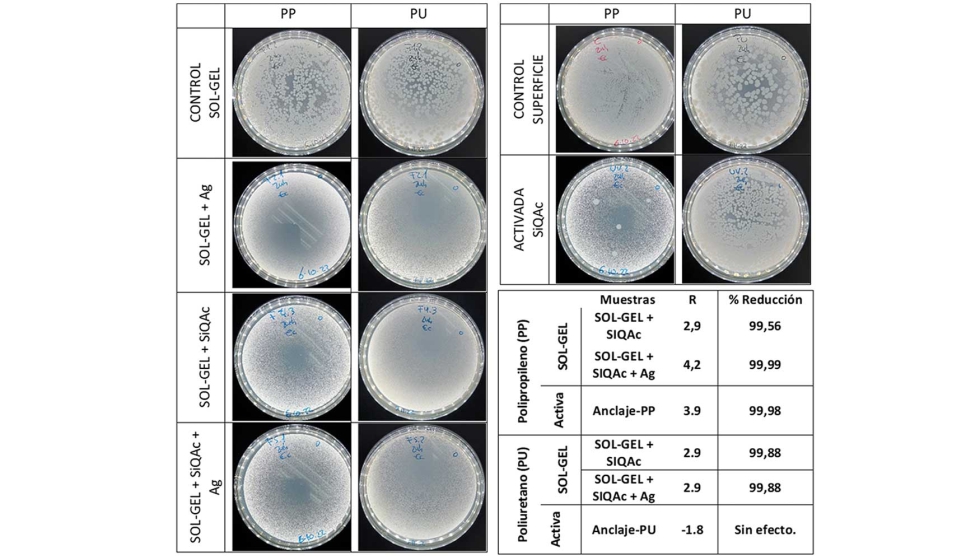
Figura 9. Imágenes del primer lavado de la evaluación antimicrobiana de las superficies poliméricas tras su funcionalización con SiQAc en ambas estrategias seguidas y en ambos materiales. En la imagen de la izquierda, los resultados tras la estrategia de recubrimiento sol-gel sin y con agentes bactericidas. En la imagen superior de la derecha, las muestras según la estrategia de activación + anclaje. En el cuadro de la derecha inferior, se muestran todos los valores cuantitativos expresados en porcentaje de eliminación de bacterias.
Conclusiones
La aplicación de nanotecnología sobre sustratos fabricados con tecnología 3D permite crear superficies modificadas con una funcionalización bactericida. La tecnología aplicada dependerá de la naturaleza del sustrato. En el caso de los metales se ha demostrado que para el Titanio se puede aplicar el anodizado electroquímico, obteniendo superficies nanoestructuradas con propiedades fotocatalíticas. Para el caso de los polímeros de polipropileno y poliuretano se pueden utilizar tanto la tecnología de funcionalización directa por enlace covalente como el recubrimiento tipo sol-gel.
Los sistemas desarrollados tienen su campo de aplicación principal en la higienización del entorno, pudiendo aplicarse para el diseño de filtros de aire, protección de material sanitario o prevención de contaminación microbiana en superficies de alto contacto en sectores tan diversos como automoción, sanitario, mobiliario urbano/doméstico o telefonía.
Este trabajo forma parte de los resultados del proyecto FILTAIR con número de expediente, IMDEEA/2021/13, financiado por la Generalitat Valenciana a través del Instituto Valenciano de Competitividad Empresarial (IVACE) y con financiación de la Unión Europea a través del Fondo Europeo de Desarrollo Regional (FEDER), dentro del programa de proyectos de I+D en cooperación con empresas 2021.
Referencias
[1] ASM International, ASM Handbook, Volume 2, Properties and Selection: Non Ferrous Alloys and Special-Purpose Materials, ASM International the Materials Information Company, Materials Park, OH, USA, 1990.
[2] M. Ma, M. Kazemzadeh-Narbet, Y. Hui, S. Lu, C. Ding, D.D. Chen, R.E. Hancock, R. Wang, Local delivery of antimicrobial peptides using self-organized TiO2 nanotube arrays for peri-implant infections, J. Biomed. Mater. Res. A 100 (2012) 278285.
[3] Izmir, M., Ercan, B. Anodization of titanium alloys for orthopedic applications. Front. Chem. Sci. Eng. 13, (2019) 2845. https://doi.org/10.1007/s11705-018-1759-y.
[4] Regonini, D., Bowen, C. R., Jaroenworaluck, A., & Stevens, R. (2013). A review of growth mechanism, structure and crystallinity of anodized TiO2 nanotubes. Materials Science & Engineering R - Reports, 74(12), 377-406. https://doi.org/10.1016/j.mser.2013.10.001.
[5] A. Lamberti, A. Virga, A. Chiadò, a. Chiodoni, et al., Ultrasensitive Ag-coated TiO2nanotube arrays for flexible SERS-based optofluidic devices, J. Mater. Chem. C 3 (2015) 68686875.
[6] A. Lamberti, N. Garino, A. Sacco, S. Bianco, A. Chiodoni, C. Gerbaldi, As-grown vertically aligned amorphous TiO2 nanotube arrays as high-rate li-based microbattery anodes with improved long-term performance, Electrochim. Acta 151 (2015) 222229.
[7] H.L. Cui, W. Zhao, C.Y. Yang, et al., Black TiO2 nanotube arrays for high-efficiency photoelectrochemical water-splitting, J. Mater. Chem. A 2 (2014) 86128616.
[8] D. Kuang, J. Brillet, P. Chen, et al., Application of highly ordered TiO2 nanotube arrays in flexible dye-sensitized solar cells, ACS Nano 2 (2008) 11131116.
[9] A. Massa, A. Lamberti, et al., Electro-oxidation of phenol over electrodeposited MnO x nanostructures and the role of a TiO 2 nanotubes interlayer, Appl. Catal. B: Environ. 203 (2017) 270281.
[10] X. He, Y. Cai, H. Zhang, C. Liang, Photocatalytic degradation of organic pollutants with Ag decorated free-standing TiO 2 nanotube arrays and interface electrochemical response, J. Mater. Chem 21 (2011) 475480.
[11] B. Ercan, E. Taylor, E. Alpaslan, T.J. Webster, Diameter of titanium nanotubes influences anti-bacterial efficacy, Nanotechnology 22 (2011) 295102.
[12] Thomson, T. Polyurethanes as Specialty Chemicals: Principles and Applications; CRC Press: Boca Raton, FL, USA, 2004.
[13] Chattopadhyay, D.K.; Raju, K. Structural engineering of polyurethane coatings for high performance applications. Prog. Polym. Sci. 2007, 32, 352418.
[14] Y. Jiao, L. Niua, S. Maa, J. Li, F. R. Tayd, J. Chena, Quaternary ammonium-based biomedical materials: State-of-the-art, toxicological aspects and antimicrobial resistance. Progress in Polymer Science 71 (2017) 5390.
[15] Jain A, Duvvuri LS, Farah S, Beyth N, Domb AJ, Khan W. Antimicrobial polymers. Adv Health Mater 2014; 3: 196985.







































