Estabilidad tartárica: origen, tratamientos y determinación analítica
El ácido tartárico es el principal componente ácido y el de mayor fuerza tanto en la uva, como en el mosto y el vino. Si bien el ácido como tal es muy soluble en agua (1.470 g/L) y algo menos en alcohol (196 g/L), son algunas de sus sales las que presentan características de insolubilidad. Históricamente tanto griegos como romanos confundieron el ácido tartárico con el cremor tártaro que se encontraba en forma de cristales en el vino. No fue sino hasta el año 1769 que el científico sueco-alemán Carl Wilhelm Scheele (descubridor del oxígeno y el nitrógeno del aire, entre otros elementos y compuestos) logró aislar el ácido tartárico.

Dentro del mosto o el vino, el potasio (K) y el calcio (Ca) son los compuesto metálicos presentes en mayor cantidad. Ambos provienen generalmente del suelo de la viña, aunque también pueden tener su origen en los distintos tratamientos realizados en el terreno y, en algunos casos, en sustancias que son añadidas durante el proceso de vinificación. El K se encuentra en su nivel más alto en la uva y luego puede ir bajando durante la fermentación alcohólica y, fundamentalmente, por los tratamientos de estabilización; pudiendo variar su contenido entre 200-2.000 mg/L. El Ca, por su parte, se encuentra presente en cantidades menores, que pueden rondar entre 40-150 mg/L. Ambas sustancias tienen la particularidad de generar sales insolubles del ácido tartárico: el bitartrato de potasio (KHT) y el tartrato de calcio (CaT), dando origen así a uno de los problemas más comunes del vino durante su período de embotellado: la aparición de sedimentos. Al ser más frecuente encontrar precipitados de KHT que de CaT, históricamente se ha estudiado la estabilidad tartárica desde el punto de vista del potasio.
Conocer a ciencia cierta la posibilidad que un vino pueda llegar a desarrollar este defecto o no y elaborar estrategias de tratamiento tendientes a despejar este riesgo son los dos puntos críticos que los enólogos encuentran durante su trabajo en bodega. En este artículo, se propone hacer un repaso de los fundamentos químicos que dan origen a la precipitación del tartárico, los tratamientos disponibles en la actualidad para intentar eliminar o reducir el riesgo de aparición de precipitados durante la comercialización y los métodos analíticos desarrollados para la determinación de la estabilidad tartárica.
Principios químicos de la estabilidad tartárica
Por sus características químicas de ácido débil, el tartárico en solución coexiste en 3 formas químicas distintas: ácido tartárico sin disociar (H2T), ion bitartrato (HT-) e ion tartrato (T2-). Las ecuaciones químicas de disociación del ácido se resumen a continuación, donde Ka1 y Ka2 son la primer y segunda constante de disociación del tartárico, respectivamente. Estas constantes dependen fundamentalmente de la temperatura.
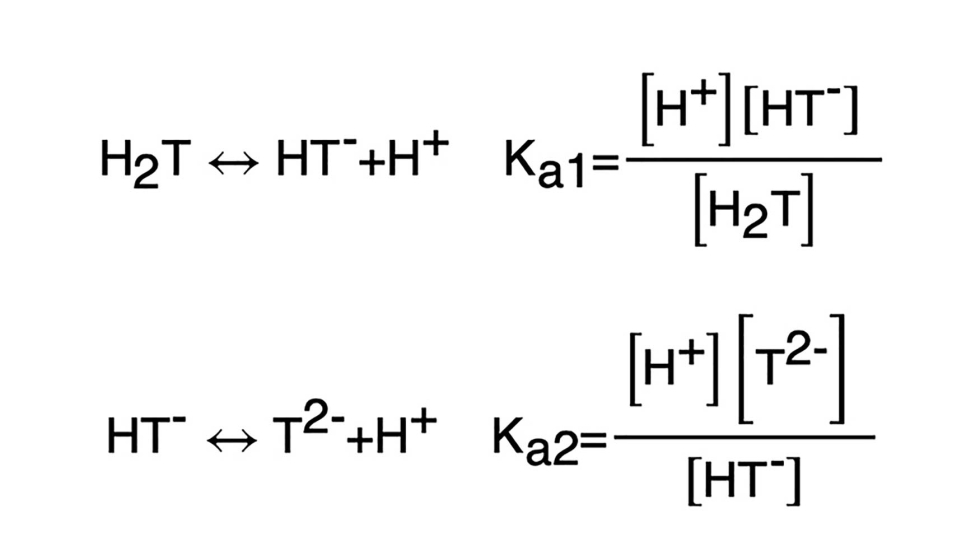
La Figura 1 muestra la distribución porcentual de estas especies en función del pH del medio de disolución a temperatura ambiente. En condiciones normales de pH de un vino, se observa que gran parte del ácido tartárico se encuentra en forma de bitartrato. Una característica interesante que surge de este diagrama es el punto de corte de las curvas de H2T y T2- a un valor de pH de aproximadamente 3,65.
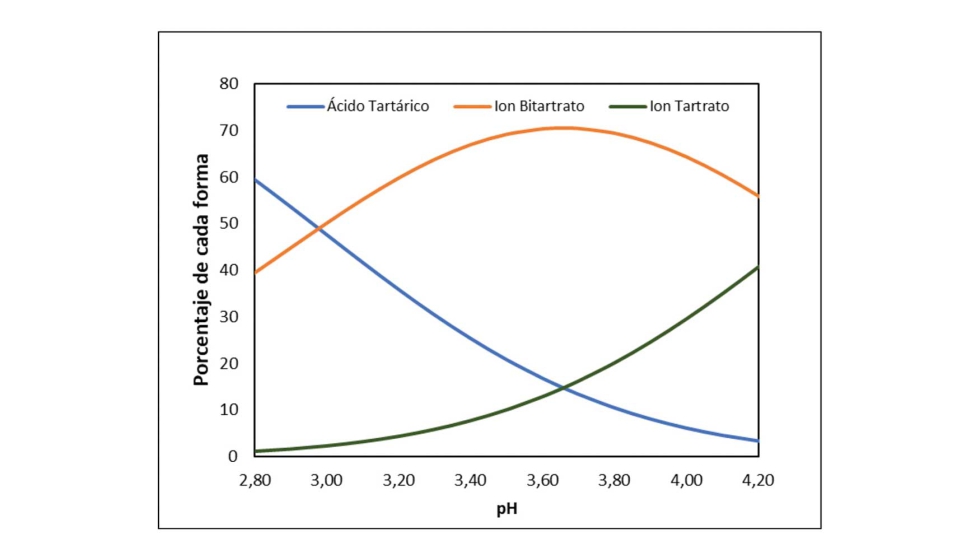
Al ubicarse en la zona de la derecha del diagrama (valores de pH>3,65), las especies mayoritarias son los iones HT- y T2-. El principio de Le Chatelier predice que, ante cualquier perturbación externa del equilibrio, el medio responderá intentando cancelar esa distorsión para volver a la situación de equilibrio. Por tanto, una precipitación de bitartrato (HT-), que retiraría este ion del medio, generaría un desplazamiento del segundo equilibrio de disociación hacia la izquierda para reponer el bitartrato. Como resultado, se estarían consumiendo iones H+ del medio generando un aumento del pH.
Por otra parte, cuando se está en la zona izquierda del diagrama (valores de pH<3,65), las especies mayoritarias son H2T y HT-. En este caso, una precipitación de bitartrato generaría un desplazamiento del primer equilibrio de disociación hacia la derecha para reponer el HT-, liberando más iones H+ al medio y, en consecuencia, reduciendo el pH.
Como puede verse, el efecto de la precipitación de bitartrato sobre el valor de pH del vino depende del pH inicial del vino, aunque en ambos casos se observará una reducción de la acidez total valorable debido a la disminución de la especie HT-.
Además de los equilibrios de disociación del ácido, para analizar la estabilidad tartárica debemos tener en cuenta los equilibrios de precipitación de las sales insolubles KHT y CaT, como se describe a continuación, donde Kps,KHT y Kps,CaT son las constantes de productos solubilidad del KHT y del CaT, respectivamente. Estas constantes también dependen de la temperatura.
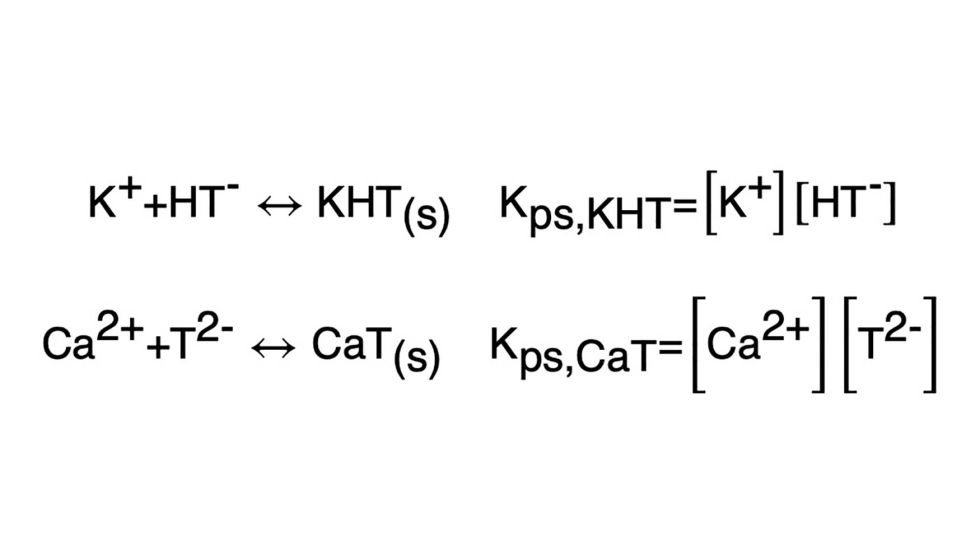
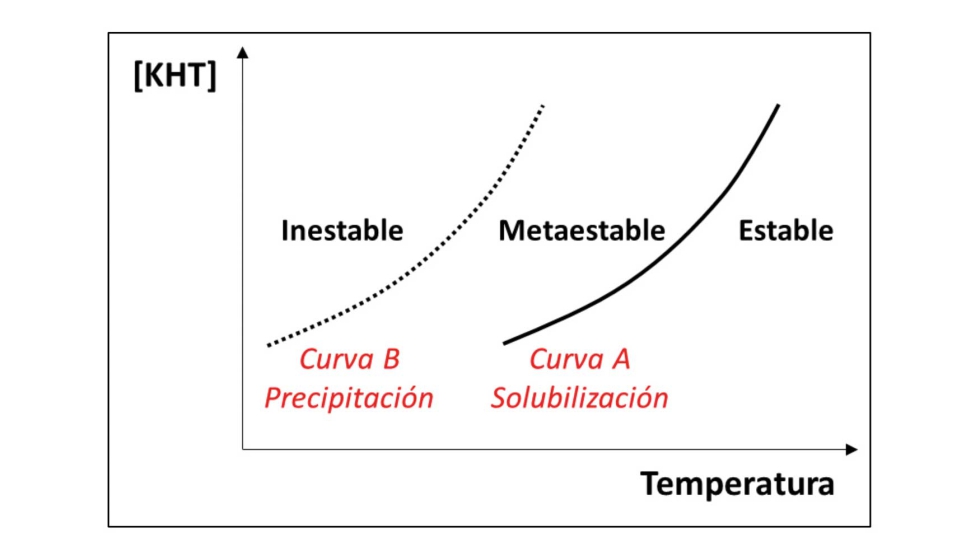
Ahora bien, todas estas constantes se suelen describir en bibliografía para soluciones acuosas puras, mientras que el vino es una mezcla de diversas sustancias. Como se puede desprender de los datos brindados en la introducción, el KHT es menos soluble en una solución hidroalcohólica como el vino que en el agua. Por otra parte, respecto a una solución agua-etanol pura el vino puede mantener una mayor cantidad de KHT en solución, debido fundamentalmente a la presencia natural de compuestos como proteínas, polifenoles y polisacáridos que pueden impedir o retardar la nucleación y el crecimiento de los cristales. Esto explica que usualmente en los vinos estemos en una situación de sobresaturación, es decir que exista más KHT en disolución que lo que la teoría marca. La Figura 2 muestra el esquema de sobresaturación. Aquí se distinguen 3 zonas:
- Zona estable: a temperaturas elevadas o concentraciones bajas de KHT, no hay riesgo de precipitación. Para un contenido dado de KHT, la temperatura de saturación (cruce con la curva A) marca la temperatura de equilibrio a partir de la cual el vino puede disolver más KHT.
- Zona metaestable: es una zona con riesgo de precipitación ya que la concentración de KHT es mayor a la solubilidad (curva A). La existencia de microcristales generaría una precipitación, lo cual depende fundamentalmente de la presencia o no de inhibidores. Si bien la curva A se puede determinar teóricamente, la curva B depende del medio y las cantidades de inhibidores presentes.
- Zona inestable: por encima de la curva B, a temperaturas bajas o cantidades elevadas de KHT, se produce la precipitación.
Operaciones de estabilización del vino
Aunque ninguna de las sales que pueden precipitar en el vino provocan daño alguno en la salud del consumidor, el principal problema que acarrean es económico: los sedimentos dañan la imagen del vino, hacen bajar la percepción de calidad del comprador y repercuten en las posibilidades de venta y en el precio. Por estos motivos, la estabilización del vino en forma previa a su embotellado y conservación, se ha vuelto una de las prácticas más comunes y más ampliamente estudiadas de la industria vinícola.
Existen diversas opciones para estabilizar el vino, que se presentan de manera resumida a continuación:
- Estabilización por frío: consiste en mantener el vino a temperaturas cercanas a los -4 °C durante largos períodos de tiempo (que pueden ser semanas) para lograr la cristalización y precipitación del KHT, para posteriormente filtrarlo en frío. Para facilitar la nucleación y crecimiento, se suelen adicionar cristales finos de KHT (0,2 g/L).
- Estabilización por contacto: consiste en refrigerar el vino a 0 °C y adicionar KHT (4 g/L), mientras se lo mantiene bajo agitación durante 4-8 horas. En este caso baja el coste energético, pero se incrementa el costo de KHT, aunque existe la posibilidad de reutilizarlo.
- Estabilización por uso de aditivos protectores: consiste en agregar al vino sustancias coloidales capaces de inhibir o ralentizar la nucleación y crecimiento de los cristales. Con este objetivo, se puede emplear ácido metatartárico, carboximetilcelulosa, poliaspartato de potasio, goma arábiga o manoproteínas. Las dosis recomendadas y requisitos de uso dependen del producto comercial utilizado.
- Estabilización mediante resinas de intercambio iónico: consiste en hacer pasar una parte del vino a tratar a través de resinas insolubles que remplazan los iones K+ por iones H+, es decir cambian el KHT menos soluble por H2T más soluble.
- Estabilización por electrodiálisis: consiste en separar los iones del vino a través del uso de membranas selectivas y la aplicación de corriente eléctrica que obliga a los cationes (como el K+) a migrar a través de ellas. El consumo eléctrico de esta técnica puede ser hasta 8 veces menor al tratamiento por frío.
Métodos para estimar la estabilidad tartárica debida al potasio
Métodos tradicionales
La primera experiencia que puede venir a la mente para determinar la estabilidad tartárica de un vino es simular las condiciones en que se llevaría a cabo la precipitación. Este test se basa en mantener el vino previamente filtrado a -4 °C de temperatura durante un tiempo variable entre 3 y 6 días. Si transcurrido este tiempo, se observa la presencia de cristales en el fondo del vino esto es un indicativo de inestabilidad. En el caso de vinos tintos, podría ocurrir una precipitación de pigmentos y taninos, que se podría distinguir del bitartrato de potasio, pues se disuelven fácilmente a temperatura ambiente.
En una variante a este método, el vino es sometido a ciclos de refrigeración de duración determinada (unas 12 horas) y posterior calentamiento a temperatura ambiente (aprox. 1 hora). Si en alguno de estos ciclos se observa un precipitado que vuelve a disolverse a temperatura ambiente, se considera que el vino es estable.
El problema de este tipo de métodos es que los resultados que brinda no son muy fiables porque dependen de la agudeza visual del observador y los microcristales podrían pasar desapercibidos.
Métodos del producto de solubilidad
Consiste en analizar el equilibrio de disolución de las sales desde el punto de vista teórico fisicoquímico. Por ejemplo, analizando la ecuación de precipitación del KHT y comparando el valor de la Kps, KHT con el valor obtenido de multiplicar las concentraciones reales de bitartrato y potasio (producto de solubilidad). Si el valor obtenido es superior a la Kps, KHT existe riesgo de precipitación. En bibliografía, se pueden encontrar valores de la constante Kps, KHT para distintos niveles de alcohol y temperatura. Por otra parte, para calcular las concentraciones de las sustancias involucradas podríamos utilizar las siguientes técnicas:
- HPLC o análisis colorimétrico automático para el ácido tartárico total.
- Análisis de pH para obtener la concentración de H+ y saber la cantidad de ion bitartrato presente.
- Absorción atómica, fotometría de llama o análisis colorimétrico automático para obtener el contenido en K+.
El resultado obtenido de esta manera sería una aproximación a la realidad, porque las ecuaciones que se presentaron anteriormente sólo se aplican en lo que en química se denomina condiciones ideales: donde cualquier propiedad termodinámica de la mezcla es igual a la suma de los aportes individuales de los componentes en función de su concentración.
Por lo tanto, las ecuaciones suben un nivel de complejidad al incorporar el coeficiente de actividad química (γ), que representa la desviación del comportamiento real de la solución frente al ideal:
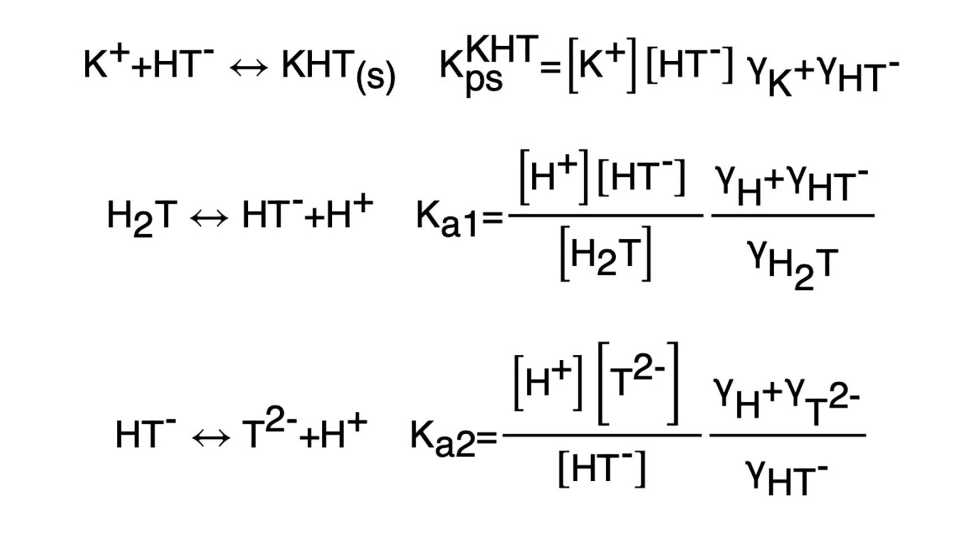
Como se dijo anteriormente, los valores de las diferentes constantes de equilibrio químico dependen fundamentalmente de la temperatura. Sin embargo, los valores de los coeficientes de actividad de cada sustancia son más difíciles de obtener, pues se deben modelar a partir de ecuaciones derivadas de la teoría de Debye-Hückel, que son del tipo:
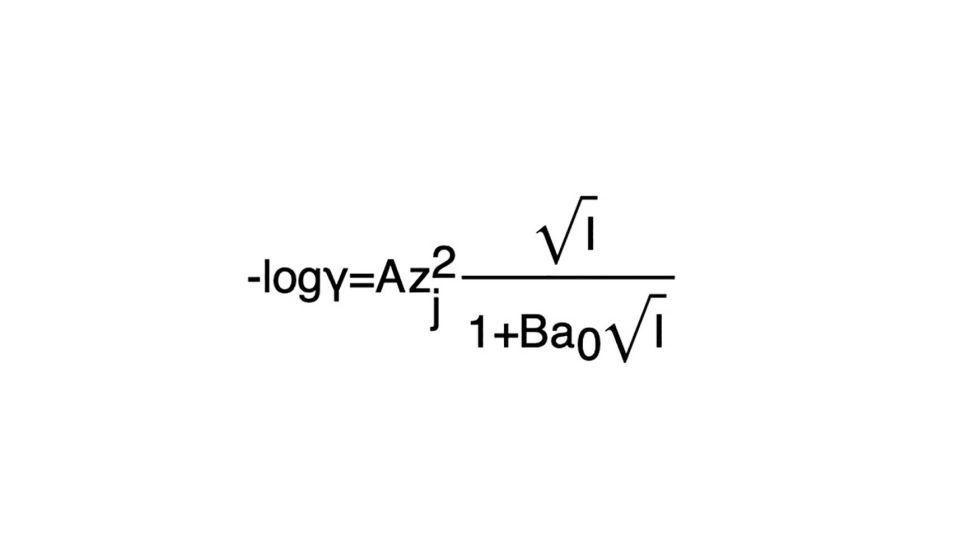
Con A y B denominadas Constantes de Debye-Hückel y que dependen del solvente y la temperatura, zj la carga de los iones, I la fuerza iónica que depende de la concentración de iones en el vino y a0 un parámetro que representa la distancia de aproximación más cercana de los iones.
Como se verá, ya no es un cálculo sencillo que puede hacerse en menos de un minuto, sino que requiere de cierta información o la toma de hipótesis, para finalmente realizar los cálculos utilizando alguna herramienta informática de complejidad media.
Métodos de medición de la conductividad
Consiste en medir la conductividad de una muestra de vino a una cierta temperatura (variable entre -4 y 5 °C, según el estilo de vino y el autor del ensayo) antes y después del agregado de una cierta dosis de KHT, que actúa como facilitador de la cristalización. Si la conductividad de la muestra baja es evidencia de una precipitación de bitartrato. En función de esta caída de la conductividad, se habla de vinos estables o inestables según si la bajada es mayor o menor al 3-5%.
Método de determinación de la temperatura de saturación
Existen dos versiones de este método.
En una primera versión, se mide la conductividad del vino a temperatura ambiente, antes y después de un agregado conocido de KHT. Al disolverse el KHT la conductividad se verá aumentada. Conociendo la conductividad inicial y final, se puede relacionar esta diferencia con la cantidad inicial de KHT en el vino y, finalmente, con la temperatura de saturación del mismo.
En una segunda versión, más sofisticada, se realizan dos tipos de medida. En primer lugar, se debe enfriar el vino hasta una cierta temperatura (entre -4 y 0 °C) y luego se registra la variación de la conductividad con el aumento de la temperatura hasta la temperatura ambiente (25 °C). Se vuelve a enfriar el vino y esta vez se le adiciona una cantidad de KHT correspondiente a 4 g/L. Nuevamente, se registra la variación de la conductividad con la temperatura hasta llegar a los 25 °C. Con ambas curvas de conductividad colocadas en un mismo gráfico, el punto de cruce entre ambas determina la temperatura de saturación. Es un método más lento que el anterior debido a las diferentes etapas de calentamiento/enfriamiento pero que tiene una fuerte base teórica detrás.
Criosmart 2: el nuevo sistema analítico para la determinación de la estabilidad tartárica
Fruto de años de experiencia y desarrollo dentro de la compañía, TDI lanzará al mercado durante este año la nueva versión del analizador de estabilidad tartárica: el Criosmart 2, presentado en la foto. Esta actualización de hardware y software muestra un diseño compacto y robusto, ideal para ocupar pequeños espacios en las bancadas de laboratorio, y presentado en los colores corporativos que han representado históricamente a TDI.

La determinación de la estabilidad tartárica se basa en la medida de la conductividad de la muestra y la utilización de cristales de KHT para favorecer la nucleación y crecimiento y generar la perturbación externa necesaria para salir de la zona metaestable. Así, el equipo posee una celda para la medición de la conductividad eléctrica, una tapa para evitar proyecciones de líquido con un pequeño agujero para el agregado manual del KHT, un mecanismo de agitación magnética y un sistema para la refrigeración y calentamiento automático de la muestra a analizar con seguimiento y detección de la temperatura.
El Criosmart 2 permite realizar de forma automática hasta tres versiones diferentes de los tests de estabilidad descritos anteriormente, de acuerdo a las necesidades del laboratorio y las características propias del vino.
Test de estabilidad ISO
Consiste en refrigerar el vino a baja temperatura, normalmente 0 o -4°C, y medir la conductividad. A continuación, el usuario deberá añadir el THK en exceso y se registrará la variación de conductividad durante un cierto tiempo, usualmente 10 minutos. En pantalla puede observarse este registro en línea.
El exceso de KHT proporciona los sitios necesarios de nucleación y crecimiento para superar la fase metaestable. Si el vino tuviera capacidad de seguir solubilizando KHT, la conductividad aumentaría por la mayor presencia de iones. Si el vino estuviera al límite de solubilidad, la conductividad no se vería modificada. Finalmente, si el vino fuera inestable se produciría una precipitación del KHT y, por tanto, la conductividad disminuiría. En general, se considera que una caída de la conductividad de entre 70-80 µS/cm es indicador de falta de estabilidad.
Test de temperatura de saturación (Ts)
Consiste en llevar el vino a una temperatura seleccionada, normalmente 25 °C, y medir la conductividad de la muestra. Posteriormente, se le pide al usuario que añada KHT y se registra la conductividad de la muestra de manera continua durante un cierto intervalo de tiempo preestablecido (normalmente 10 minutos). A esta temperatura, se observará un aumento de la conductividad debido a la solubilización del KHT. La relación entre los valores de conductividad inicial y final permiten determinar un valor de Ts de acuerdo a ecuaciones ya programadas en el software. La experiencia se puede repetir a 30 °C si el valor de la Ts fuera igual a 25 °C. En general, si el valor de la Ts es menor a 7°C, los resultados no son muy fiables y se debería determinar el valor de saturación a través del método descrito a continuación.
Test de temperatura de saturación estable (Tss)
Consiste en determinar la temperatura a la cual la solubilidad del KHT es igual a la concentración del KHT presente en la muestra de vino. Como se reprodujo anteriormente, este método consiste de varias etapas:
- En primer lugar, se refrigera el vino hasta la temperatura mínima y, una vez estable, se calienta la muestra mientras se registra la variación de la conductividad con la temperatura, en un rango normalmente de -4 a 25°C y que debe incluir la Ts.
- En segundo lugar, se vuelve a refrigerar el vino hasta la temperatura mínima. Una vez estable, se le pide al usuario que añada un exceso de KHT.
- Finalmente, se vuelve a calentar la muestra en el mismo rango de temperatura, mientras se registra de manera continua la conductividad.
Mientras la primera curva de conductividad es lineal porque esta solo depende de la temperatura, la segunda curva tiene una forma diferente. En este caso, la conductividad no aumenta solo por la temperatura, sino que también por solubilización del KHT. Si el vino está en la zona metaestable, cuando la temperatura de la muestra está por debajo de la Ts, poco o nada de KHT se solubiliza porque no hay capacidad. Sin embargo, por encima de la Ts el KHT sí se solubilizará y la diferencia entre las curvas será mayor. Este fenómeno se utiliza para encontrar el valor de la temperatura de saturación estable (Tss), que representaría la temperatura a partir de la cual sería termodinámicamente posible que el vino sufra algún tipo de precipitación tartárica.
Desde hace más de 39 años, TDI se encarga de prover a laboratorios y bodegas de soluciones analíticas a medida para resolver los problemas más habituales de los enólogos. Con la mente puesta en brindar al cliente el mejor servicio pre y posventa, ponemos todos nuestros canales de comunicación a disposición de clientes y usuarios para recibir el mejor y más honesto asesoramiento en la elección del equipo ideal. No lo dudes y ¡súmate a la enolución!

