Rol de los compuestos nitrogenados en el vino y su análisis
Las principales formas químicas presentes en el mosto son los aminoácidos, los péptidos, las proteínas y el ion amonio. Otros compuestos químicos nitrogenados de menor importancia incluyen los nitratos, los nitritos, los nucleótidos, las vitaminas, las aminas y las amidas. En la Tabla 1, se muestran resultados orientativos obtenidos de la literatura.
| Compuesto |
Concentración en mostos (mg N/L) |
|
Nitrógeno Total |
40-2.400 |
|
Ion Amonio |
10-250 |
|
Ion Nitrato |
<10 |
|
Aminoácidos |
30-350 |
| Péptidos |
20-500 |
| Proteínas |
4-90 |
|
Aminas biógenas |
< 50 |
La cantidad exacta de cada una de estas familias de compuestos nitrogenados varía ampliamente al comparar mostos y vinos obtenidos provenientes de distintas variedades de uvas, de diferentes regiones, e incluso dentro de la misma región según los tratamientos que se hayan podido aplicar en el viñedo. Así, en literatura se puede encontrar que el contenido total de nitrógeno varía entre 40-2.400 mg N/L. De la misma manera, los valores para el contenido en amonio oscilan entre 19-250 mg N/L y para el contenido en aminoácidos entre 28-336 mg N/L. Además, el perfil individual de aminoácidos es extremadamente variable entre las distintas variedades de uva y las diferentes regiones, aunque en general se puede decir que el más abundante de ellos es la prolina y, a continuación, la arginina, la alanina, el glutamato, la glutamina, la serina y la treonina, en un orden que puede sufrir modificaciones entre las distintas fuentes consultadas.
Dentro de los muchos factores que influyen en la variabilidad encontrada al analizar el contenido en compuestos nitrogenados, los más importantes son: la variedad de uva, el portainjerto, el nivel de madurez de la uva al momento de la cosecha, el tipo de suelo, el clima, la utilización o no de compuestos nitrogenados como fertilizantes en el viñedo y la presencia de infecciones de tipo fúngicas. No menos importantes son los diversos tratamientos a los que se somete la uva para la obtención del mosto y que pueden modificar en forma directa o indirecta (a través de la proliferación de microorganismos) los niveles de nitrógeno analizados: el prensado, los tratamientos enzimáticos, la clarificación, la filtración, los tratamientos con bentonita, los tratamientos térmicos, por nombrar algunos de ellos.
La importancia de conocer el nivel de compuestos nitrogenados presentes en el mosto radica fundamentalmente en la influencia directa que tienen en la cinética de fermentación. Las fermentaciones lentas y las súbitas paradas de fermentación se suelen asociar a la existencia de déficits en el contenido de nitrógeno del mosto. Esto se debe al rol esencial de estos compuestos en el metabolismo y el crecimiento de las levaduras: sin nitrógeno no se pueden construir los bloques fundamentales para el crecimiento de un organismo vivo. Además, los compuestos nitrogenados son un factor clave en los mecanismos de formación de los precursores aromáticos que dotarán luego al vino de su aroma y olor.
De manera usual, la uva se suele cosechar teniendo en cuenta parámetros de madurez tecnológica y/o fenólica, que no suelen coincidir con los niveles óptimos de nitrógeno para una fermentación adecuada. Por esto, se suele recurrir a la utilización de suplementos nitrogenados, que si bien alteran la composición inicial del mosto, facilitan el crecimiento óptimo de las levaduras. Si bien hay diversas fuentes y productos comerciales en base a nitrógeno utilizables en bodega, el fosfato diamónico es el compuesto de uso más extendido para este fin debido a temas de costo, facilidad de manejo y rapidez de asimilación por parte de las levaduras. Sin embargo, en algunos casos es necesario también suplementar el mosto utilizando fuentes de tipo orgánico que nos aseguren la provisión de compuestos esenciales como aminoácidos y vitaminas. Finalmente, la utilización de urea está prohibida en varios países debido a su implicación en la formación de carbamato de etilo en el vino, un compuesto sospechoso de tener actividad carcinogénica.
Sumado a todo lo anteriormente dicho, hay que tener en cuenta que no todas las fuentes de nitrógeno son accesibles de igual manera por la levadura e incluso, algunas de ellas, no lo son en absoluto. Para que la levadura pueda hacer uso de los compuestos nitrogenados es necesario que éstos entren a la célula a través de algún tipo de mecanismo de transporte. Por esta razón, las formas nitrogenadas preferidas por las levaduras corresponden a dos grupos: los aminoácidos primarios (que representan la fracción orgánica del N) y las sales del ion amonio (que representan la fracción inorgánica del N). La prolina, el aminoácido más abundante en los mostos, no es asimilable por las levaduras debido a que es un aminoácido secundario.
La suma de ambas fracciones utilizables constituye lo que se denomina el nitrógeno fácilmente asimilable (NFA), también conocido como nitrógeno asimilable por las levaduras (YAN, por sus siglas en inglés). El NFA determinado en las uvas es un valor indicativo de poca utilidad práctica, porque la mayoría de los compuestos nitrogenados están en la piel y para pasar al mosto debe haber algún tipo de contacto entre ellos. Por esta razón, es indispensable determinar el NFA en el mosto antes de comenzar la fermentación para determinar si es necesario realizar algún tipo de suplementación. Los mostos con niveles iniciales de NFA inferiores a 150 mg N/L suelen dar lugar a fermentaciones muy lentas con baja población de levaduras. Por otra parte, niveles excesivamente elevados de NFA conducen a poblaciones de levaduras anormalmente altas, lo cual genera una mayor temperatura de fermentación y una mayor producción de acidez volátil, además del riesgo de producción de aminas biógenas. Además, altos niveles de NFA también pueden favorecer el desarrollo de microorganismos no beneficiosos debido a la mayor disponibilidad de nutrientes. Adicionalmente al control inicial, será necesario mantener una vigilancia de los niveles de NFA a lo largo de todo el proceso fermentativo como herramienta de control para evitar paradas indeseadas y para determinar si es necesario realizar suplementaciones adicionales.
Por todo lo detallado, el seguimiento del valor de NFA se torna en un elemento indiscutible para el control del proceso y la obtención de vinos de alta calidad y precio. A continuación, se repasarán las técnicas existentes para la determinación de los niveles de nitrógeno en mostos y vinos, de acuerdo a dos grandes tipos de análisis basados en la determinación del nitrógeno total o del fácilmente asimilable.
Métodos de determinación del contenido total de nitrógeno
Este tipo de métodos se encuentran oficializados por la Organización Internacional de la Viña y el Vino (OIV) en su Compendio Internacional de Métodos de Análisis. Allí se recogen dos tipos de métodos para la determinación cuantitativa del contenido de nitrógeno total.
El primero de ellos (OIV-MA-AS323-02A) se basa en el principio químico del método de Dumas. En un primer momento la muestra es sometida a una combustión total en atmósfera de oxígeno. Luego, los gases generados durante la combustión se reducen utilizando cobre y se procede a desecarlos y eliminar el dióxido de carbono presente en ellos. Finalmente, el nitrógeno gaseoso es detectado utilizando un catarómetro.
El segundo tipo de método (OIV-MA-AS323-02B) se basa en el principio químico del método de Kjeldahl. En este procedimiento la muestra se digiere en primer lugar utilizando ácido sulfúrico en presencia de un catalizador específico (mezcla de sulfato cúprico y potásico). Posteriormente, en una segunda etapa, se somete el producto de la digestión a una destilación en medio alcalino. De esta manera, el amoníaco generado se recoge en el destilado para luego ser determinado por valoración utilizando para tal fin una solución de ácido clorhídrico 0,1M.
La principal desventaja de este tipo de métodos, además de lo laborioso que son, es que ambos determinan el contenido total de nitrógeno y por tanto valoran en exceso el nitrógeno que realmente está disponible a nivel biológico para las levaduras.
Métodos de determinación del nitrógeno fácilmente asimilable (NFA)
Existen diversos métodos para determinar el NFA, es decir, la suma del contenido en ion amonio y en aminoácidos primarios de una muestra de mosto o vino. Algunos de estos métodos realizan la determinación conjunta mientras que otros realizan una determinación por separado de cada una de las fracciones en consideración. Si se recuerda la definición del NFA, éste podía representarse como la suma de una contribución de origen orgánico (aminoácidos primarios libre, conocidos como PAN o FAN por sus siglas en inglés) y otra de origen inorgánico (ion amonio). Cada una de estas fracciones cuenta con métodos de determinación específico. Se repasa cada una de las opciones a continuación.
Método de Sorensen para la determinación conjunta del NFA
En este método, con el fin de bloquear los iones amonio y los grupos amino de los aminoácidos presentes la muestra es inicialmente tratada con una solución de formaldehído (también llamado formol). De esta manera, se dejan libres los contraiones ácidos de las sales de amonio y los respectivos grupos carboxilo de los aminoácidos. En consecuencia, el pH de la muestra disminuye y la acidez resultante puede ser determinada mediante valoración con solución de hidróxido de sodio 0,1M. Es importante tener en cuenta que, tanto la muestra como la solución de formaldehído, tienen que estar previamente ajustadas a un pH igual a 8 para poder llevar a cabo una determinación precisa y sin interferencias.
El dióxido de azufre, habitualmente presente en las muestras de vinos y mostos, puede alterar el resultado obtenido debido a su función ácida, particularmente si las dosis son muy altas. Esta interferencia puede evitarse realizando una defecación previa de la muestra con solución de cloruro de bario.
Si bien esta valoración no tiene en cuenta el contenido de prolina entre los aminoácidos que se determinan, existen diversos compuestos que pueden llegar a interferir en la determinación y, por tanto, suelen obtenerse valores en exceso respecto a los otros métodos de determinación del NFA.
Durante años el método Sorensen fue la manera habitual de determinar el NFA en mostos y vinos. Sin embargo, la complejidad de la técnica, que precisa de cierta habilidad manual del operador, sumada a las condiciones especiales necesarias para trabajar con un compuesto tóxico como el formaldehído, han llevado a la práctica desaparición de esta técnica de los laboratorios enológicos.
Métodos para la determinación del ion amonio
Cabe decir que la OIV cuenta con un método oficial para la determinación del ion amonio (OIV-MA-AS-322-01) basado en la fijación del analito de interés a través del uso de una resina de intercambio iónico para su posterior elución, destilación y valoración final con una solución de ácido clorhídrico. Sin embargo, en la práctica es un método demasiado complicado y laborioso para ser utilizado de rutina. Es por esto que con el transcurso del tiempo surgieron varias alternativas. Algunas de ellas, como la determinación mediante electrodos de iones selectivos, también demostraron ser poco prácticas. Por otra parte, la determinación enzimática del ion amonio ha probado con creces ser la mejor y más eficiente técnica para la medición del contenido de amonio en muestras de vino y mostos.
El principio químico de la técnica enzimática se basa en la determinación selectiva y específica del ion amonio a través de su reacción con el ion 2-oxoglutarato en presencia de la enzima glutamato deshidrogenasa y del cofactor NADPH, como se muestra en la Figura 1.

Aprovechando las características de absorbancia del cofactor NADPH, es posible realizar un seguimiento espectrofotométrico de esta reacción a través de la lectura de la absorbancia de la mezcla a 340 nm.
La utilización de patrones de concentración conocida para efectuar la calibración siguiendo la ley de Lambert-Beer, el empleo de reactivos líquidos y estables a largo plazo como los suministrados por TDI y la aparición hace ya un tiempo de los analizadores químicos automáticos, de los cuales la gama Miura es su mayor exponente, facilitan al operador todas las tareas de manejo de reactivos, calibración y cálculo de las concentraciones a determinar en las muestras incógnitas.
Métodos para la determinación de los aminoácidos primarios
Existen varios métodos químicos utilizados en la derivatización de aminoácidos para su determinación conjunta por espectrofotometría UV-Vis o para su determinación individual a través de métodos de separación como la cromatografía de líquidos (HPLC). Entre los compuestos químicos capaces de reaccionar con los aminoácidos y, por tanto, de ser útiles para su determinación, se pueden nombrar a: la ninhidrina, el o-ftalaldehído (OPA), el fenilisotiocianato, el ácido 2,4,6-trinitrobencenosulfónico, el cloruro de dansilo, entre otros.
A nivel práctico para las bodegas, la posibilidad de contar con equipos de HPLC y de esperar los largos tiempos de análisis que son necesarios para cada muestra, limita la aplicabilidad de esta técnica de manera rutinaria, limitándola sólo a actividades de investigación.
Por otro lado, la utilización y variedad de analizadores químicos automáticos disponibles en el mercado, como puede verse en la Figura 4 que presenta la gama completa de analizadores Miura, ha permitido extender el uso de la espectrofotometría UV-Vis a laboratorios de bodegas de todos los tamaños.
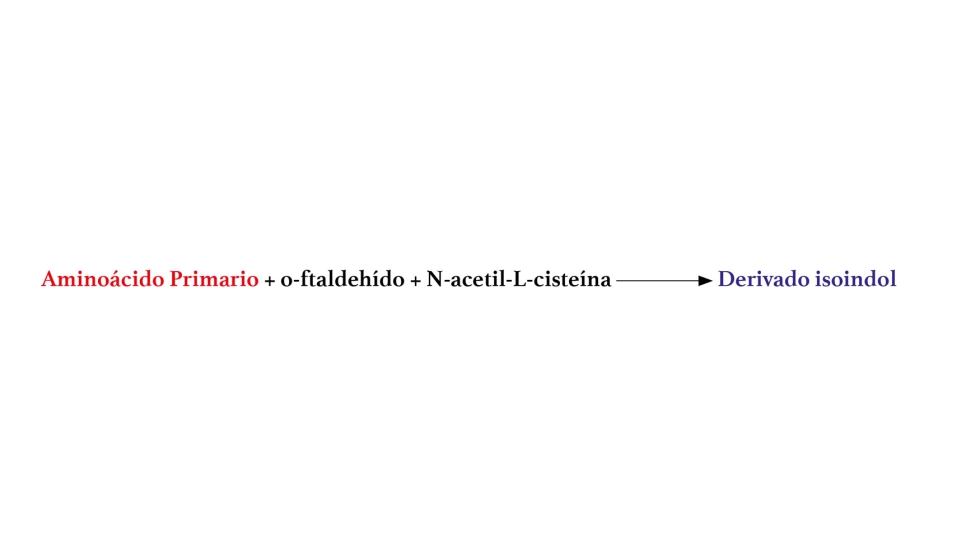
Al respecto de esta técnica, cabe decir que su desarrollo comenzó en 1998 en la Universidad de California en Davis (Estados Unidos) debido al trabajo de Christian Butzke sobre un método para la determinación de los aminoácidos primarios consistente en la derivatización de éstos con un reactivo de o-ftalaldehído y N-acetil-L-cisteína, como se muestra en la Figura 2. Este reactivo es capaz de formar un derivado de tipo isoindol con cada uno de los aminoácidos de interés, pudiendo determinarse fácilmente a través de la medición de la absorbancia de la mezcla a 340 nm. En su trabajo inicial, sin embargo, la estabilidad de los reactivos de determinación apenas llegaba a un par de semanas. Actualmente, los reactivos desarrollados y comercializados por TDI presentan una alta estabilidad (18 meses) manteniendo e incluso mejorando las prestaciones analíticas, gracias al uso de materias primas de alta calidad y de patrones estables de concentración conocida. De esta manera, se facilita la determinación de la fracción orgánica del NFA.
Conclusión
El avance tecnológico en la construcción y diseño de los analizadores químicos automáticos, sumado a la investigación y desarrollo en la producción de reactivos químicos enzimáticos y colorimétricos más estables, permiten hoy en día a las bodegas poder disponer de valores de NFA fiables y en poco tiempo, sin tener que recurrir a metódicas tediosas, trabajosas y de resultados cuya practicidad queda en duda.
De esta manera, TDI apuesta por la simplificación del trabajo y la facilidad en el uso de las técnicas analíticas más modernas, permitiendo liberar el tiempo del operador para otras tareas, evitando la complejidad del manejo de sustancias tóxicas y/o peligrosas y contribuyendo a facilitar la tarea diaria del enólogo, que sólo debe responsabilizarse de tomar las decisiones adecuadas para obtener el mejor de los vinos.
Si posee una necesidad analítica y desea saber cómo resolverla, no dude en comunicarse con nosotros vía mail (info@t-d-i.es), a través de la web www.tdianalizadores.com o de nuestras redes sociales, y juntos podremos encontrar la mejor solución.
Más de 35 años de experiencia enológica nos avalan, no lo dude y ¡súmese a la enolución!


