Biomateriales para el par articular de las prótesis de cadera
La aparición de determinadas enfermedades ligadas a esta articulación como la artritis, entre otras, induce a los traumatólogos en muchos casos a realizar una artroplastia total de cadera como método para recuperar la calidad de vida del paciente. En la actualidad el número de pacientes en todo el mundo al que se le implanta este tipo de prótesis se aproxima al millón por año.
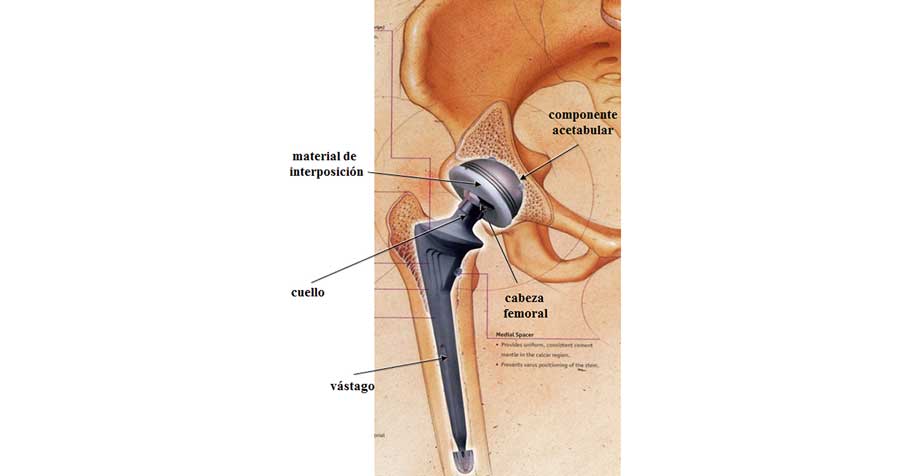
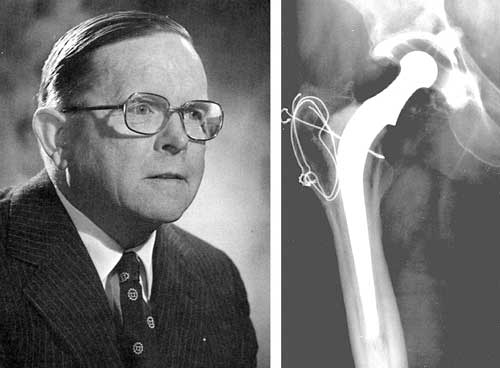
En la imagen 1 se muestran los elementos de una de estas prótesis, que está formada por la componente femoral y el vástago que pueden formar un monobloque o ser elementos diferentes, y la componente acetabular que se une a la pelvis. Además, entre la cabeza y la componente acetabular puede existir un material de interposición que se denomina copa o liner en inglés. El diseño de este tipo de prótesis fue introducido a finales de los años 60 por Sir John Charnley del Wrigthtington Hospital en el Reino Unido (Figura 2), y se puede considerar en parte una evolución de las prótesis Austin Moors y McKee-Ferra.
Sin embargo, mientras que el diseño de esta prótesis ha permanecido hasta nuestros días sin demasiados cambios relevantes, los biomateriales que forman parte de la misma han evolucionado fuertemente acompañados del desarrollo que la Ciencia y Tecnología de Materiales ha experimentado en este último medio siglo. Para hacernos una idea, materiales como el marfil, caucho, resina acrílica, vidrio, baquelita o pirex fueron algunos de los materiales utilizados como constituyentes de la cabeza femoral en la primeras décadas del siglo XX, sin que el comportamiento a largo plazo fuera el deseable, por lo que no forman parte de las actuales prótesis.
La dificultad de encontrar materiales idóneos viene impuesta por un conjunto de exigencias sobre el implante que los agentes reguladores como la FDA de los EE UU o las directivas europeas imponen. No es fácil encontrar, entre los miles de aceros y aleaciones, una cantidad superior de polímeros, a los que hay que sumar las cerámicas y los materiales compuestos, los materiales que cumplen con los requerimientos establecidos. Muchos de estos materiales cumplen con las exigencias de rigidez, resistencia a la tracción, compresión y flexión, y buen comportamiento a fatiga, que son algunas de las prestaciones mecánicas necesarias para soportar las cargas durante la actividad diaria de la articulación. Sin embargo la biocompatiblidad exigida al material condiciona y restringe el número de materiales implantables a una docena aproximadamente, entre los que se incluyen tres familias de aleaciones basadas en hierro, cobalto y titanio, un polímero como el polietileno, y las cerámicas inertes alúmina y circona. La biocompatibilidad que manifiestan estriba en una alta resistencia a la corrosión que impide que los iones metálicos se lixivien y terminen en la sangre, y también en que las partículas metálicas, poliméricas y cerámicas que se puedan generar en el desgaste entre las superficies articulares de la prótesis no introduzcan una bioactividad negativa en el cuerpo humano. De ahí que las propiedades tribológicas sean también una exigencia para que estos materiales presenten una sostenibilidad de las prótesis con probabilidades de supervivencia del 90-95 % en periodos de quince o veinte años.
Si focalizamos la atención en los materiales del par articular, nos encontramos con que las prótesis más extendidas actualmente, 70-80 % del mercado, son las metal-polietileno, con la cabeza femoral de metal (acero inoxidable 316 L o la aleación de Co-Cr-Mo) y la copa de polietileno de ultra alto peso molecular (PEUAPM), y las de cerámica-polietileno con cabezas de Al203 o ZrO2.
El primer par metal-polietileno fue introducido por Sir John Charnley en 1963. Los metales utilizados fueron los existentes en aquella época, el acero inoxidable 316L y la aleación CoCrNiMo. El primero contiene un bajo contenido en carbono, inferior al 0,03 %, para evitar la sensibilización del acero, y los aleantes Cr, Ni, Mo contribuyen a mejorar la resistencia a la picadura, hendidura y a corrosión bajo tensión, aspectos que no se controlan exclusivamente con la presencia de la capa de pasivación de Cr2O3. En los años 80s apareció el acero 316L denominado Orthinox, con un contenido de nitrógeno mayor, que potencia la resistencia a la corrosión. Aun siendo notables las características de estos aceros, sus prestaciones son inferiores a las de la segunda aleación, CoCrNiMo, que apareció en implantes de cadera en 1939, un año después de la introducción del acero inoxidable en Traumatología y Cirugía Ortopédica. Esta aleación no sólo tiene una excelente resistencia a la corrosión, sino que presenta un comportamiento a fatiga superior, con un límite de fatiga entre 600 y 900 MPa, casi el doble que el acero inoxidable sin alto contenido en nitrógeno. Estas aleaciones con base Co obtienen sus altas prestaciones mecánicas debido a que se pueden endurecer por diversos mecanismos como la distribución uniforme de carburos precipitados, un tamaño de grano pequeño o la presencia de dos fases. Junto a estas ventajas hay que añadir que pueden ser conformadas tanto por fundición como por forja, si bien su precio es más alto que el del acero 316L.
Las ventajas que esas aleaciones metálicas aportaban como cabeza femoral a las prótesis, se vieron potenciadas con la introducción por S. Charnley del PEUAPM en la copa, después de un intento fallido de utilizar como contrapar el politetrafluoretileno, PTFE, de coeficiente de fricción muy bajo, hecho en el que se fundamentaba el diseño de su prótesis. Este polietileno presenta buenas características mecánicas, bajo coeficiente de fricción, buena resistencia a desgaste y alta biocompatibilidad. Parte de estas propiedades descansan en la estructura de cadenas poliméricas con alto grado de polimerización (2-6x 106 g/mol) que posee este polímero semicristalino en el que una misma cadena forma parte de varias lamelas o regiones cristalinas. Sin embargo, el desgaste que experimenta el polietileno frente al metal, aun no siendo considerable desde el punto de vista que afecte dimensionalmente a la función de la prótesis, lo es respecto a la bioactividad que producen las partículas submicroscópicas que se generan y que dan lugar a un proceso de pérdida de hueso periprotésico denominado osteolisis. Este proceso genera aflojamiento y es una causa importante de la revisión de prótesis. La reticulación de las cadenas poliméricas mediante la radiación gamma o haces de electrones es la clave que permite disminuir el desgaste del polietileno. Para ello se utiliza una dosis de radiación entre 50 y 100 kGy, muy superior a la de 25 kGy que fue utilizada a partir de finales de los años 60 para esterilizar las copas de polietileno. Estos polietilenos altamente reticulados deben ser sometidos posteriormente a tratamientos térmicos de recocido o refusión, o a la incorporación de 0,001 % de vitamina E (Figura 3) para reducir los radicales libres que induce la radiación y que generan, al cabo de varios años, un proceso oxidativo con fragilización del material. Este polietileno no ha estado exento de cambios microestructurales con resultados negativos, como los que salieron al mercado con grados de cristalinidad del 60 % y que, a pesar de cumplir con las ensayos de desgaste pertinentes, su comportamiento no fue satisfactorio ya que el desgaste ¨in vivo¨ fue superior al determinado en ensayos in vivo. La orientación de las cadenas de polietileno en los ensayos unidireccionales en el laboratorio fue la razón de esa diferencia de comportamiento tribológico.
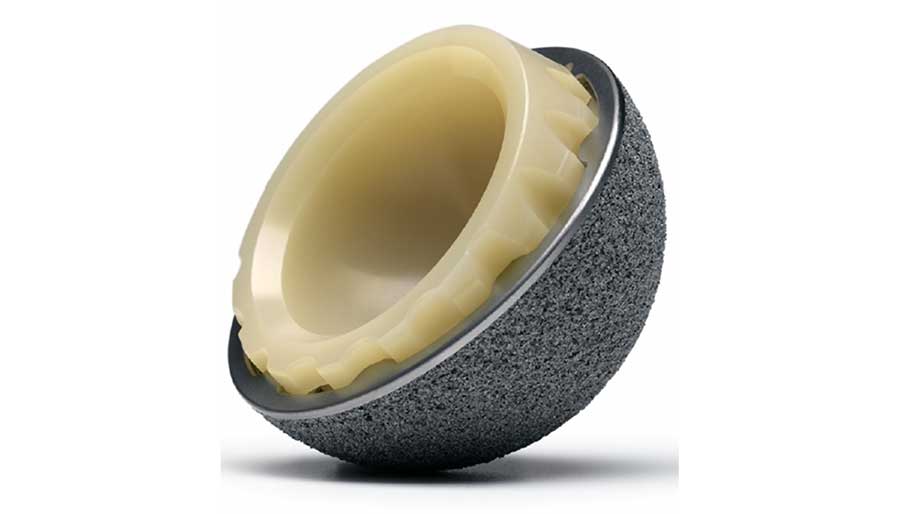
Una alternativa actual al PEUAPM, aunque con una cota de mercado muy minoritaria, la constituye el policarbonato uretano como material de interposición (Figura 4). Este polímero es más hidrófilo que el PEUAPM, lo que permite establecer una lubricación de película de fluido, y su comportamiento elastomérico presenta propiedades mecánicas próximas a la de los cartílagos. La reducción de espesor de la copa para obtener cabezas de fémur con mayor diámetro que impidan la dislocación pasa por incrementar las propiedades mecánicas del PEUAPM, reforzándolo con fibras de carbono (Poly II) con resultados dudosos como hace unas dos décadas, o los intentos actuales de refuerzo mediante nanotubos de carbono o grafeno.

La aparición del par metal-polietileno, redujo fuertemente la presencia del par CoCrNiMo-CoCrNiMo, pero éste continuó utilizándose debido al menor desgaste que experimentaban estas prótesis. Este aspecto se potenció con la aparición de la segunda generación de cabezas y acetábulos que presentan una esfericidad casi perfecta y una rugosidad media por debajo de 0,01 micras minimizando el desgaste abrasivo (Figura 5). Por otra parte, la potencial bioactividad de las partículas metálicas de desgaste de unas 0,03 micras no se han manifestado hasta la fecha, a pesar del aumento en el contenido de determinados iones en la sangre que no alcanzan niveles de toxicidad. No es el caso de algún modelo concreto de prótesis de superficie de cadera (Figura 6) con implantación en pacientes jóvenes y activos, cuyo diseño generó durante su uso necrosis tisulares y severa inflamación en un porcentaje relativamente alto. Su retirada del mercado en 2010, acarreó en algunos países, particularmente EEUU, una opinión negativa injustificada sobre el uso de las habituales prótesis con pares metal-metal.

Los pares articulares en los que interviene la alúmina fueron introducidos en 1960 y rápidamente su implantación fue restringida por fallos por fractura. La baja tenacidad de la cerámica fue determinante frente a otras propiedades altamente positivas, como la dureza, el bajo desgaste, la densidad o el carácter hidrófilo que permite una lubricación por película de fluido. Desde el principio de la década de los años 90, la tenacidad de la alúmina se ha visto incrementada por medio de varios mecanismos (Figura 7), como un menor tamaño de grano, próximo a 1-2 micras, una porosidad del 0,1 % como consecuencia de la utilización de procesos de sinterización por presión isostática en caliente, la inclusión de circona estabilizada con itrio para aprovechar la transformación de fase inducida por tensión o la presencia de placas de óxido de estroncio que dificulta el avance de las posibles grietas. El resultado es una tenacidad que prácticamente evita la fractura y produce un desgaste próximo a 1 mm3/106 ciclos, inferior al generado por los pares del polietileno altamente reticulado frente al metal (9 mm3/106 ciclos) o a la cerámica (4 mm3/106 ciclos).


El desarrollo de los materiales en estas últimas décadas ha permitido que las actuales prótesis de cadera presenten una vida operativa más larga, al solventar algunas de las causas que producen una revisión de la prótesis, intervención que genera una alta carga emocional al paciente e incluso riesgo personal, además de un coste económico para la sociedad. Otros aspectos de la prótesis como los materiales idóneos para los vástagos, los recubrimientos para una fijación no cementada en el vástago y en la componente acetabular para una buena osteointegración, el comportamiento de la adhesión bacteriana en la superficie de los biomateriales, la sustitución de elementos químicos por otros de menor toxicidad en los materiales metálicos, son otros de los temas de investigación que mejorarán las prestaciones de las futuras prótesis de cadera.
José Antonio Puértolas Ráfales es Catedrático del Área de Ciencia de Materiales e Ingeniería Metalúrgica de la Universidad de Zaragoza y responsable del Grupo de Biomateriales del Instituto de Investigación en Ingeniería de Aragón (I3A).