Últimos avances tecnológicos en Urología
Los conocimientos de la anatomía y de las patologías urológicas han permitido avanzar en la búsqueda de tecnología que permitiera, no sólo ampliar el conocimiento en torno a las mismas, sino la curación y el tratamiento de los pacientes. En las últimas décadas son muchas las innovaciones que han cobrado protagonismo en la urología, la más novedosa, desde el punto de vista tecnológico, ha sido el robot quirúrgico.
Las enfermedades prostáticas
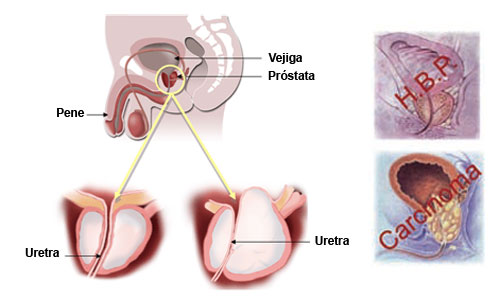
Los avances técnicos en relación con las patologías de la glándula prostática (ver figura 1) hay que centrarlos, indiscutiblemente, en dos procesos: la hiperplasia benigna de próstata y el carcinoma de próstata. Para abordar las patologías prostáticas es imprescindible nombrar a personalidades tan relevantes como los doctores Salvador Gil-Vernet, Charles Huggins, McNeal, Watanabe, Gleason, Wang o Patrick Walsh.
Salvador Gil-Vernet nació en Vandellós (Tarragona) en 1893 y falleció en Barcelona en 1987. Dedicó su vida fundamentalmente a la docencia de la anatomía y más concretamente de la anatomía quirúrgica lo que hoy denominamos anatomía traslacional y a la investigación.
Desarrolla la anatomía aplicada a la cirugía o, lo que es lo mismo, la anatomía quirúrgica. A través de su investigación anatómica de carácter traslacional llega a la conclusión de que la glándula prostática tiene dos partes: una central que corresponde a la glándula craneal, y una parte periférica, la glándula caudal. La relevancia radica en que en la glándula craneal es donde se va a desarrollar el proceso hiperplásico, mientras que en la caudal se genera el carcinoma de próstata. Estos datos están recogidos en la obra 'Patología y biología de la próstata', editada en tres volúmenes publicados en la Editorial Paz Montalvo en Madrid, 1953.
Fue presidente de la Sociedad Internacional de Urología desde 1967 a 1973, académico de honor de esta Real Academia Nacional de Medicina y miembro de honor de la Asociación Española de Urología. Ha tenido numerosos reconocimientos, como el del propio Ramón y Cajal, el del profesor Flock de la Universidad de Iowa y el de Charles Brenton Huggins, que le propuso para el Nobel de Medicina. Es digna de referir la editorial que el profesor Ruano le hace con motivo de su fallecimiento.
El segundo hombre relacionado con la patología prostática es Charles Brenton Huggins (1901-1997), urólogo de la Universidad de Chicago que renunció a la actividad clínica y se dedicó a la investigación. Él demostró la hormona-dependencia del cáncer de próstata, estudios por los que le concedieron el Premio Nobel de Medicina en 1966. Otro urólogo reseñable es el doctor Werner Forssman (1904-1979) de la Facultad de Medicina de la Universidad de Berlín, también Nobel de Medicina en 1956, por ser el primero en realizar un cateterismo cardíaco con un catéter ureteral.
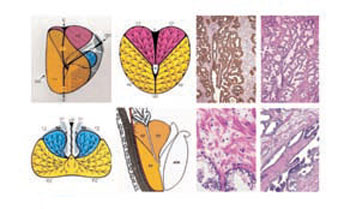
El tercer nombre al que hay que hacer referencia es John E. McNeal, que al igual que Gil-Vernet interpretó la glándula prostática (ver figura 2). Mientras que Gil-Vernet lo hace desde un punto de vista global, McNeal lo hace posteriormente desde un punto de vista zonal. En la zona periférica es donde se desarrolla fundamentalmente el cáncer de próstata y, a veces, en la zona de transición, donde generalmente se desarrolla la hiperplasia benigna de próstata. Los datos que describen la morfología y patología de la glándula prostática fueron publicados en el Medical Journal Clinical Pathology en 1968.
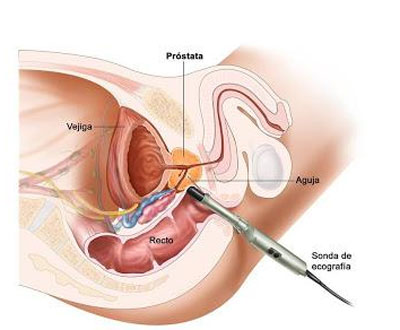
Un aspecto imprescindible a la hora de abordar la glándula prostática son los estudios a través de los ultrasonidos, de alta y baja frecuencia. Estos últimos son los que nos permiten valorar el riñón, la vejiga y la próstata. En cambio, los de alta frecuencia, que tienen un bajo poder de penetración pero una alta resolución, nos permiten observar la glándula prostática mediante la introducción del transductor en el recto. Fue el Profesor H. Watanabe quien descubrió y diseñó este tipo de transductor de alta frecuencia, que ha sido tan importante para estudiar la morfología de la próstata y, muy especialmente, para poder dirigir la aguja de biopsia (ver figura 3). Actualmente, ésta se lleva a cabo con un pistola automática que permite una mayor precisión a la hora de tomar la muestra.
Otro aspecto de interés clínico es qué zona de la glándula hay que biopsiar. Tradicionalmente se decía que se debían pinchar aquellos nódulos de carácter anecoico, es decir, de menor econogenicidad. Recientemente se ha demostrado que se debe pinchar cualquier tipo de nódulo: anecoico, isoecoico, hipoecoico e, incluso, hiperecoico, excepto aquellos nódulos hiperecoicos con sombra acústica posterior compatibles con litiasis. Posteriormente se publicaron una serie de trabajos en los que se recomendaban seis cilindros, es decir, biopsia sextante. El doctor Stamey, por su parte, aconsejó que las muestras-biópsicas fueran lo más periféricas posibles. Por otro lado, cuanto más número de cilindros se obtengan más probabilidades de localizar el cáncer hay, pero también esto conlleva una mayor morbilidad.
El doctor Donald Gleason, patólogo de la Universidad de Minneapolis en Minnesota, investiga el grado de diferenciación celular del cáncer de próstata y lo relaciona con el estadio y el pronóstico. Distingue cinco grados de diferenciación celular y establece la escala que lleva su nombre, que divide a los pacientes en 3 grupos: el primer grupo lo constituyen aquellos pacientes que tiene un score de Gleason entre 2 y 4; el segundo, los que tienen un score 5-6; y el tercero, un score de Gleason entre 7 y 10.
La distinta incidencia y prevalencia del cáncer de próstata en relación a los países del este de Asia con respecto a Estados Unidos, Canadá y Nueva Zelanda indujo al profesor M.C. Wang del Roswell Park Cancer Institute de Búfalo a investigar un marcador que permitiera hacer el diagnóstico de forma precoz. Sus investigaciones lo llevan a describir el PSA, el Antígeno Prostático Especifico, una glicoproteína que es fabricada fundamentalmente por la glándula prostática. Los estudios fueron publicados en el Investigative Urology en el año 1979. Esta glicoproteína se incrementa en la hiperplasia de próstata, el cáncer de próstata y la prostatitis, por ello es un marcador muy sensible pero poco específico.
Finalmente, otro nombre fundamental en la investigación de la glándula prostática es el doctor Patrick Walsh, el primero que, con la colaboración de un anatómico de la Universidad de Lieja, sistematizó la cirugía del cáncer de próstata: la prostatectomía radical.
Sobre la glándula prostática también se desarrolla un proceso hiperplásico benigno que hace que dicha glándula aumente de volumen y conlleve trastornos miccionales, representados por el prostatismo o los síntomas del tracto urinario inferior. Su tratamiento es farmacológico, pero si éste falla, hay que optar por un tratamiento más invasivo: la adenomectomía y la resección transuretral. En relación con estos procedimientos quirúrgicos hay que tener en cuenta aspectos relacionados con la estancia hospitalaria, el tiempo de sondado, la necesidad de transfusión o la posibilidad de complicaciones, como la incontinencia urinaria o la impotencia.
Estos parámetros también han sido valorados a la hora de emplear el láser (luz mediante la estimulación por la emisión de radiación. Los resultados obtenidos, en algunos casos, son mejores. Los láser más empleados en la Urología son el Ho:YAG, el ND:YAG y el KTP. Algunos de ellos también nos permiten resolver otros procesos urológicos. Por ejemplo, antes del láser se empleaba un cuchillete frío en las estenosis de uretra para llevar a cabo una uretrotomía interna, que en muchas ocasiones conllevaba una reacción fibrosa importante que hoy en día se puede evitar empleando estas nuevas tecnologías.
El segundo proceso en el que se puede emplear el láser es en la resección o ablación de la glándula prostática, el carcinoma de pene o los tumores vesicales, para los que también se van a utilizar el láser diodo y el láser CO2.
En tercer lugar, se usa también en el tratamiento de la litiasis, en la litotricia de cálculos de pelvis renal, de uréter y de vejiga. En estos casos se emplea fundamentalmente el láser Ho:YAG, el láser diodo y el láser alexandrita.
Finalmente, el láser también puede ser utilizado en otros procesos, como sería la soldadura de tejidos en las vasostomías, en la reconstrucción uretral o en la hipospadia, en la autofluorescencia a través del láser de nitrógeno, en el diagnóstico de tumores uroteliales y en la eliminación del vello para llevar a cabo las uretroplastias con parche o con colgajo de piel escrotal.
La patología vesical
En relación con la patología vesical, los avances que se han producido en las últimas cinco décadas comienzan con el tratamiento del carcinoma in situ a través de la BCG (Bacilo de Calmette-Guerin). El segundo aspecto de interés es la derivación urinaria destubulizada. Desde que se utilizara por primera vez el intestino como sistema de sustitución vesical en el carcinoma vesical infiltrante, al que se le ha llevado a cabo una cistectomía, se ha avanzado mucho.
En 1969, en la Universidad de Goteborg (Suecia), el cirujano Nils Koc introdujo el concepto de destubulización, es decir, la sección del borde antimesentérico, lo que permite romper la actividad peristáltica y, en consecuencia, la elevada presión del segmento intestinal empleado. También permite mediante esa plancha de intestinos destubulizados poder hacer un modelaje y un diseño de ese reservorio.
Respecto al diseño del reservorio hay tres factores a tener en cuenta: la configuración, la adaptación y la compliance. En la configuración se intenta hacer un reservorio lo más parecido a la vejiga y la figura geométrica más parecida es la esfera. Por otro lado, la adaptación viene marcada por la fórmula de Simon Laplace, en la que la presión es igual a la tensión partida por el radio. Y la compliance es la capacidad de adaptación de la vejiga a los cambios de volumen y cambios de presión, es decir, cuanto más baja sea la presión mejor va a ser la compliance.
Litiasis urinaria
Cuando abordamos la litiasis urinaria tenemos que hablar de la cirugía más compleja de la litiasis, que es la litiasis coraliforme. El doctor José Mª Gil-Vernet estudió la anatomía del seno renal enfocada a la cirugía de la litiasis coraliforme. Esta anatomía quirúrgica, compleja pero muy resolutiva, así como sus separadores palpebrales, fueron los factores que facilitaban la cirugía intrasinusal. Siempre defendió la cirugía del seno, mucho más anatómica que la nefrotomía anatrófica, que lleva una mayor morbilidad y una destrucción más importante de nefronas (ver figura 4).
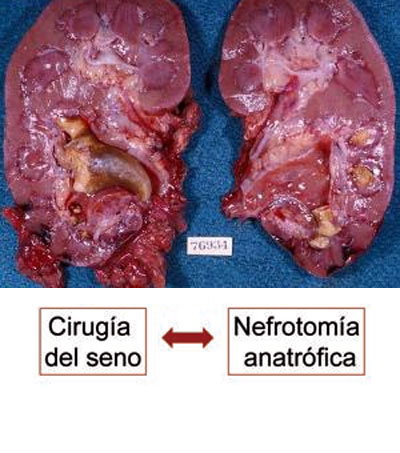
No obstante, la cirugía de la litiasis ha tenido a lo largo del tiempo y de la evolución tecnológica diferentes alternativas, como la disolución de los cálculos in situ, la litolisis química, la endourología transuretral y translumbar, que emplea diferentes formas de energía como la electrohidráulica, la ultrasónica, el láser y la energía neumática, y la litotricia extracorpórea por ondas de choque. La endourología se puede dividir en endourología percutánea o translumbar y en endourología transuretral. La endourología percutánea o translumbar se lleva a cabo mediante un nefroscopio que se introduce a través de la piel, y una vez que llega a la pelvis, a través de los distintos tipos de energía, se pueden destruir los cálculos. Por otro lado, la endourología transuretral utiliza dicha vía para poder abordar los diferentes tipos de litiasis de la vía excretora. Existen dos tipos de ureteroscopio: uno rígido y otro tecnológicamente más avanzado que es flexible.
Cabe mencionar la Litotricia Extracorpórea por Onda de Choque (LEOC o, según la terminología inglesa, ESWL), cuyo objetivo es romper los cálculos de mayor tamaño y transformarlos en pequeños cálculos que se puedan eliminar con facilidad. Esta tecnología tiene su origen en el sector aeronáutico, concretamente en la fábrica de aviones Dornier en Alemania, ya que tras ver como en la II Guerra Mundial los B-29 caían con cierta frecuencia coincidiendo con temporales, Dornier realizó diferentes experimentos. Entre ellos, observó que cuando los aviones Lockheed F-104 alcanzaban la velocidad del sonido derramaban agua sobre el fuselaje del avión y pudo comprobar que cada gota de agua producía una erosión en el fuselaje de unos 20 milímetros. Posteriormente comprobaron que esa onda expansiva no dañaba los tejidos y se pusieron en contacto con el profesor Eisenberg y con el profesor Chaussy, del Hospital Universitario de Munich, para estudiarlo a nivel experimental.
Fue el 7 de febrero de 1980 cuando se llevó a cabo la primera litotricia por onda de choque en Alemania. Estos trabajos fueron publicados en el Journal of Urology en el año 1981.
Un equipo de litotricia tiene tres sistemas fundamentales: el generador de ondas de choque, el sistema de localización del cálculo y el acoplamiento al paciente. Los generadores pueden ser electrohidráulicos, piezocerámicos y electromagnéticos. El sistema de localización del cálculo utiliza los ultrasonidos y fundamentalmente el aparato de Rayos X o la fluoroscopia. Y finalmente el acoplamiento al paciente, que hace que la expansión de la onda no pierda energía. Puesto que para ello, hace años había que sumergir al paciente en una bañera, la litotricia adquirió popularmente el nombre de la bañera.
Del ser humano al robot
Ya expresaba Miguel Ángel en la Capilla Sixtina que el hombre ha querido crear una criatura a su imagen y semejanza, por eso, ha creado un robot. En Medicina contamos con el sistema Da Vinci, que la FDA (Food and Drug Administration) aprobó para el uso en la Urología en 2001. Este sistema tiene tres partes fundamentales: los brazos articulados, la consola y la torre de monitorización.
Cuenta con cuatro brazos articulados, dos tienen una función quirúrgica, un tercero donde se encuentra la cámara de vídeo, que permite obtener imágenes estereocópicas y tridimensionales, y un cuatro brazo que sirve para separar y traccionar. Los brazos del robot permiten al cirujano operar en áreas pequeñas y realizar incisiones muy precisas, eliminando posibles movimientos involuntarios (ver figura 5). Tiene una pinza básica y otras accesorias, que se articulan de una forma similar a la mano humana.
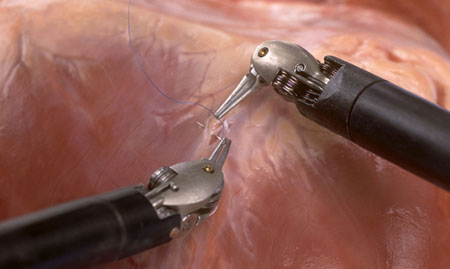
El cirujano dirige la actividad quirúrgica con detalle desde la consola, que tiene una base informática muy compleja. Como dato histórico destacamos que en 2001 se realizó una colecistectomía en la que los brazos del robot y el paciente estaban situados en un hospital de Estrasburgo, mientras que la consola y el cirujano que dirigía la operación estaban en un hospital de Nueva York. Les separaba una distancia de 7.000 kilómetros y en la imagen sólo había un retraso de 150 milisegundos.
Respecto a esta tecnología quisiera destacar dos frases: una de Vipul Patel, director general del Instituto de Robótica del Hospital de Florida, quien recientemente ha dicho: No he visto a nadie que haya hecho un número importante de cirugías robóticas regresar. La segunda es de Michael Barry, del Massachussets General Hospital de Boston, quien afirmó: Una vez que un hospital invierte en un robot 1,39 millones y 140.000 dólares al año para el contrato de servicio, médicos y pacientes se convierten en defensores apasionados. El beneficio del robot es indiscutible: disminuye el dolor, la fibrosis, al ser maniobras precisas y pequeñas la pérdida de sangre también es menor, y el paciente regresa a la actividad diaria antes.
Evidentemente también hay que valorar el tiempo de ocupación del quirófano, el número de transfusiones, la estancia postoperatoria, la retirada de sonda uretral, la continencia, la potencia sexual y, por supuesto, el gasto por intervención y mantenimiento.

El presente artículo forma parte de la ponencia que Jesús Castiñeiras Fernández, académico de número de la Real Academia de Medicina de Sevilla, catedrático de Urología de la Universidad de Sevilla y jefe de Servicio de Urología del Hospital Virgen Macarena, pronunció en la X Conferencia Innovación Tecnológica en Urología, del Ciclo de Conferencias La aportación de la Tecnología Sanitaria, organizado por la Fundación Tecnología y Salud y la Real Academia Nacional de Medicina.

